
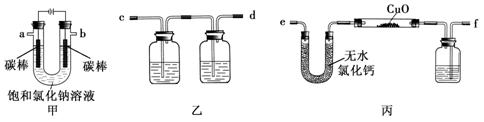
| A.淀粉碘化钾溶液 | B.NaOH溶液 |
| C.FeCl2与KSCN混合溶液 | D.Na2SO3溶液 |
 对硬质玻璃管里的氧化铜粉末加热前,需进行的操作为 。
对硬质玻璃管里的氧化铜粉末加热前,需进行的操作为 。 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:不详 题型:实验题
 学认为发生双水解反应,其反应方程式为2Fe3++3SO32-+6H2O=2Fe(OH)3(胶体)+3H2SO3;
学认为发生双水解反应,其反应方程式为2Fe3++3SO32-+6H2O=2Fe(OH)3(胶体)+3H2SO3; 应选用的试剂是 。
应选用的试剂是 。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| 编号 | 实验内容 | 实验目的 |
| A | 先加足量溴水,然后再加入酸性高锰酸钾溶液 | 要鉴别己烯中是否混有少量甲苯 |
| B | 将石油裂解气通入酸性高锰酸钾 | 确定裂解气中含有乙烯 |
| C | 淀粉溶液和稀H2SO4混合加热,后加新制的Cu(OH)2悬浊液加热至沸腾 | 检验淀粉水解产物有还原性 |
| D | 将乙醇与浓硫酸共热制得的气体通入酸性KMnO4溶液中 | 检验气体中含有乙烯 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
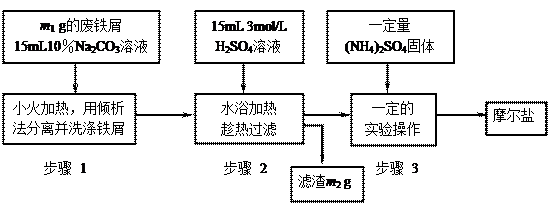
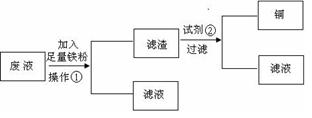
 中铁屑过量的目的是(用离子方程式表示): ▲ 。步骤2中溶液趁热过滤的原因是 ▲ 。
中铁屑过量的目的是(用离子方程式表示): ▲ 。步骤2中溶液趁热过滤的原因是 ▲ 。 加热到 ▲ 时,停止加热。需经过的实验操作包括: ▲ 、 ▲ 、减压过滤(或抽滤)等得到较为 ▲ 的晶体。
加热到 ▲ 时,停止加热。需经过的实验操作包括: ▲ 、 ▲ 、减压过滤(或抽滤)等得到较为 ▲ 的晶体。 量,一般采用在酸性下用KMnO4标准液滴定的方法。
量,一般采用在酸性下用KMnO4标准液滴定的方法。 (7)在25℃时,相同物质的量浓度的(NH4)2 CO3、(NH4)2SO4、摩尔盐三种盐溶液a,b,c,其铵根离子浓度由小到大的排列顺序为: ▲ 。(用a,b,c回答)
(7)在25℃时,相同物质的量浓度的(NH4)2 CO3、(NH4)2SO4、摩尔盐三种盐溶液a,b,c,其铵根离子浓度由小到大的排列顺序为: ▲ 。(用a,b,c回答)查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
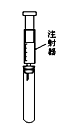
| A.试管中盛酚酞试液,验证氨气的水溶液呈碱性 |
| B.试管中盛酸性高锰酸钾溶液,探究SO2的还原性 |
| C.试管中盛稀氢氧化钠溶液, 验证CO2与NaOH反应的产物 |
| D.装置中充满NO2气体,探究压强对化学平衡的影响 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
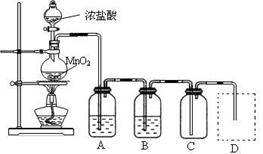
| 实验方法 | 实验现象 | 结论 |
| 在溶液中加 KSCN溶液 | | 固体物质中有FeCl3 |
| 向a溶液中滴加 酸性KMnO4溶液 | KMnO4溶液紫色 不褪色 | 固体物质中不含______ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.铝箔在酒精灯火焰上加热熔化但不滴落,说明铝箔表面氧化铝膜的熔点高于铝 |
| B.将SO2通入含HClO的溶液中,生成H2SO4,说明HC1O酸性比H2SO4强 |
| C.FeCl3溶液可以腐蚀线路板上的Cu,说明Fe的金属活动性大于Cu |
| D.乙烯和苯都能使溴水褪色,说明乙烯和苯都能和溴水发生加成反应 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
| A.用碱式滴定管取待测液NaOH溶液放入锥形瓶,滴加2—3滴酚酞指示剂。 |
| B.用待测的NaOH溶液润洗碱式滴定管。 |
| C.把滴定管用蒸镏水洗净。 |
| D.取下酸式滴定管,用标准的盐酸溶液润洗后,再将标准的盐酸注入酸式滴定管至刻 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
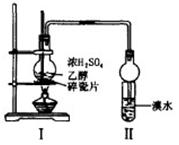
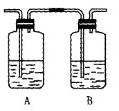
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com