
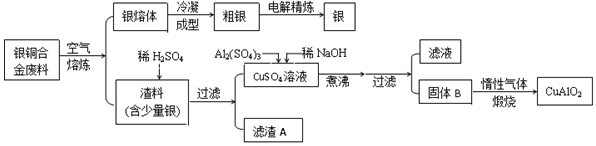
分析 由工艺流程图可知,废料在空气中熔炼时,Cu被氧化,滤渣中含有CuO及少量Ag,向滤渣中加入硫酸进行酸浸,CuO与硫酸反应,过滤得到硫酸铜溶液(含有硫酸),滤渣A为Ag;在硫酸铜溶液中加入硫酸铝、氢氧化钠,煮沸、过滤得到Al(OH)3和CuO,灼烧中会得到CuO、Al2O3,二者煅烧可得到CuAlO2,滤渣A含有Ag,粗银电解时,粗银为阳极,在阴极上得到银,可得到提纯的目的,
(1)根据电解原理分析判断,电镀法精炼银时,粗银为阳极,精银为阴极;
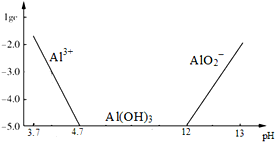
(2)依据图象和溶度积常数计算铜离子和铝离子完全沉淀所需的PH,未煮沸之前是Cu(OH)2和Al(OH)3,Cu(OH)2分解的温度为80℃判断产物,根据氢氧化铝显两性能与碱反应;
(3)根据化合价升降总数相等以及原子守恒来配平;
(4)根据铜元素守恒建立关系式:Cu~CuAlO2来计算;根据铝元素守恒建立关系式:Al2(SO4)3~2CuAlO2来计算.
解答 解:(1)电解法精炼银时,粗银为阳极,精银为阴极,电解质为硝酸银,阳极上失电子变成离子进入溶液了:Ag-e-=Ag+,阴极银离子得到电子形成单质银:Ag++e-=Ag,
故答案为:阳;AgNO3;Ag++e-=Ag;
(2)未煮沸之前是Cu(OH)2和Al(OH)3,Al(OH)3和Cu(OH)2,煮沸后Cu(OH)2分解产生氧化铜,可知B为Al(OH)3和CuO,在生成固体B的过程中,需控制NaOH的加入量,使溶液的pH范围在铝离子和铜离子全部沉淀,氢氧化铝沉淀完全PH=12,室温时,Cu(OH)2的溶度积Ksp=2.0×10-20.(lg5=0.7),据此计算全部沉淀的PH,c2(OH-)=$\frac{2×10{\;}^{-20}}{1×10{\;}^{-5}}$=2×10-15,c(H+)=10-6.65,PH=6.65,在生成固体B的过程中,需控制NaOH的加入量,使溶液的pH范围在为:6.65-12,氢氧化铝显两性能与碱反应:Al(OH)3+NaOH=NaAlO2+2H2O,反应的离子方程式为:Al(OH)3+OH-=AlO2-+2H2O,
故答案为:6.65-12; Al(OH)3+OH-=AlO2-+2H2O;
(3)反应前Cu为+2价,反应后为+1,化合价降低1,Al化合价没有变化,所以氧元素的化合价升高,生成氧气,反应前氧为-2价,反应后为0,化合价升高2,两者的最小公倍数是2,再根据原子守恒得:4CuO+2Al2O3=4CuAlO2+O2↑,
故答案为:4CuO+2Al2O3=4CuAlO2+O2↑;
(4)由关系式:Cu~CuAlO2得n(CuAlO2)=$\frac{1000g×64%}{64g/mol}$=10.0mol,则CuAlO2为10.0mol,
由关系式:Al2(SO4)3~2CuAlO2得Al2(SO4)3=n(CuAlO2)×$\frac{1}{2}$=5.0mol,所以需要体积为$\frac{5mol}{1.0mol/L}$=5L,
故答案为:5.
点评 本题为工艺流程题,从废料中回收银并制备铜化工产品为背景,考查了电解原理、沉淀的判断、氧化还原反应的配平以及化学计算,难度中等.


 全能测控一本好卷系列答案
全能测控一本好卷系列答案科目:高中化学 来源: 题型:选择题
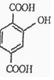
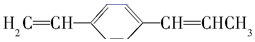 的说法正确的是( )
的说法正确的是( )| A. | 所有原子都在同一平面上 | |
| B. | 最多有4个碳原子在同一直线上 | |
| C. | 有7个碳原子可能在同一直线上 | |
| D. | 最多只能有9个碳原子在同一平面上 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
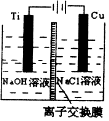 纳米级Cu2O由于具有优良的催化性能而受到关注,表为制取Cu2O的三种方法:
纳米级Cu2O由于具有优良的催化性能而受到关注,表为制取Cu2O的三种方法:| 方法Ⅰ | 用炭粉在高温条件下还原CuO |
| 方法Ⅱ | 电解法:2Cu+H2O$\frac{\underline{\;电解\;}}{\;}$ Cu2O+H2↑ |
| 方法Ⅲ | 用肼(N2H4)还原新制Cu(OH)2 |
| 序号 | 0 | 10 | 20 | 30 | 40 | 50 | |
| ① | T1 | 0.050 | 0.0492 | 0.0486 | 0.0482 | 0.0480 | 0.0480 |
| ② | T1 | 0.050 | 0.0488 | 0.0484 | 0.0480 | 0.0480 | 0.0480 |
| ③ | T2 | 0.10 | 0.094 | 0.090 | 0.090 | 0.090 | 0.090 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
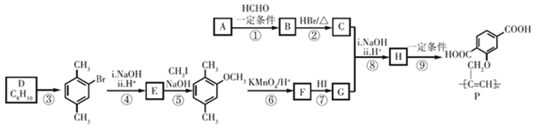
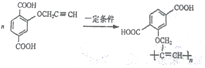
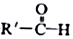 $\stackrel{一定条件}{→}$R-C≡
$\stackrel{一定条件}{→}$R-C≡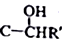
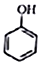 +CH2I$\stackrel{NaOH}{→}$
+CH2I$\stackrel{NaOH}{→}$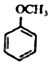 +NaI+H2O
+NaI+H2O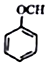 +HI→
+HI→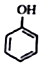 +CH2I
+CH2I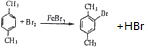 .
. .
. .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:实验题
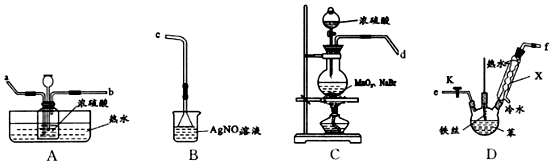
 ;仪器X的名称为球形冷凝管.
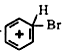
;仪器X的名称为球形冷凝管. ?
?
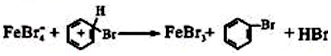 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烯通入溴的四氯化碳溶液中,溶液褪色 | |
| B. | 光照甲烷和氯气的混合气体后,瓶壁上有油状液滴附着 | |
| C. | 苯滴加到溴水中,震荡后水层接近无色 | |
| D. | 在葡萄糖溶液中加入新制的氢氧化铜,加热后产生砖红色沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | K+、CO32、AlO2- | B. | SO42-、AlO2-、K+、CO32-、 | ||
| C. | CO32-、K+、Al3+ | D. | MnO4-、K+、CO32-、NH4+ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com