
分析 根据n=$\frac{V}{{V}_{m}}$计算氯气物质的量,根据方程式计算耗Ca(ClO)2的物质的量和消耗HCl的物质的量,以及电子转移总数,由此分析解答.
解答 解:标况下,2.24L氯气的物质的量为$\frac{2.24L}{22.4L/mol}$=0.1mol,
由Ca(Cl)2+4HCl(浓)═CaCl+2H2O+2Cl2↑,可知耗Ca(ClO)2的物质的量为$\frac{0.1}{2}$=0.05mol,被氧化的Cl-为0.1mol×$\frac{1}{2}$=0.1mol,反应时电子转移的总数为0.1×6.02×1023=6.02×1022个,故答案为:0.05mol;0.1;6.02×1022.
点评 本题考查物质的量有关计算、化学方程式计算,比较基础,侧重对基础知识的巩固.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:解答题
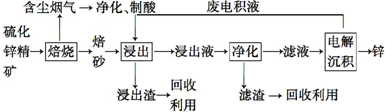
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①和② | B. | ③和④ | C. | ④和⑤ | D. | 只有③ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
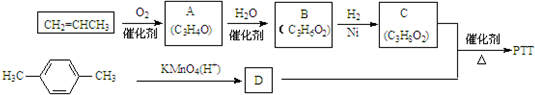
 .①分子式为C4H6O ②含有1个-CH3
.①分子式为C4H6O ②含有1个-CH3 ,反应类型为缩聚反应.
,反应类型为缩聚反应.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| t/℃ | 700 | 800 | 830 | 1 000 | 1 200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com