
| A. | 1L浓H2SO4中含有0.5gH2SO4 | B. | 0.5L含有49gH2SO4的溶液 | ||
| C. | 0.5gH2SO4溶于水配成2L溶液 | D. | 0.1L含24.5gH2SO4的溶液 |
分析 根据n=$\frac{m}{M}$计算9.8g H2SO4的物质的量,再根据c=$\frac{n}{V}$计算其物质的量浓度.
解答 解:A、1L浓H2SO4中含有0.5gH2SO4,硫酸的浓度为$\frac{0.5g}{98g/mol×1L}$=1/196mol/L;
B、0.5L含有49gH2SO4的溶液的浓度为$\frac{49g}{98g/mol×0.5L}$=1mol/L;
C、0.5gH2SO4溶于水配成2L溶液,硫酸的浓度为$\frac{0.5g}{98g/mol×2L}$=1/392mol/L;
D、0.1L含24.5gH2SO4的溶液,硫酸的浓度为$\frac{24.5g}{98g/mol×0.1L}$=2.5mol/L.
故选D.
点评 本题考查物质的量浓度计算,比较基础,侧重对基础知识的巩固.


 出彩同步大试卷系列答案
出彩同步大试卷系列答案科目:高中化学 来源: 题型:选择题
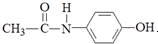 ,有关它的性质描述错误的是( )
,有关它的性质描述错误的是( )| A. | 它能与NaOH溶液反应 | |
| B. | 其水解产物之一对氨基苯酚(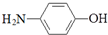 )具有弱酸性、弱碱性和强还原性 )具有弱酸性、弱碱性和强还原性 | |
| C. | 与对硝基乙苯互为同分异构体 | |
| D. | 1mol该物质与浓溴水反应时最多消耗Br23mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加水,使溶液体积变为原来的10倍 | B. | 升高温度(不考虑NH3的挥发) | ||
| C. | 加入适量的NH4Cl固体 | D. | 加入等体积0.2mol/L的氢氧化钠 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
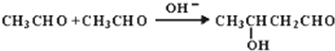

 .E中含氧官能团的名称为羟基、醛基.
.E中含氧官能团的名称为羟基、醛基.
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 只有①⑦ | B. | 除②外都是 | C. | 只有①④⑥⑦ | D. | 只有①③ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Al3+,Cl-,K+,OH- | B. | H+,Na+,SO42-,S2- | ||
| C. | Na+,Ca2+,HCO3-,OH- | D. | Mg2+,H+,SO42-,NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 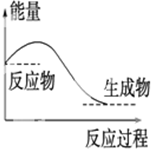 对于如图所示的过程,是放出能量的过程 | |
| B. | 由“C(石墨)=C(金刚石)”反应为吸热,可知,金刚石比石墨稳定 | |
| C. | 由水变成冰是放热反应 | |
| D. | 1 mol H2SO4与1 mol Ba(OH)2反应生成BaSO4沉淀时放出的热叫做中和热 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
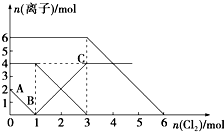 已知:2Fe2++Br2═2Fe3++2Br-,2Fe3++2I-═2Fe2++I2.向FeI2、FeBr2的混合溶液中通入适量氯气,溶液中某些离子的物质的量变化如图所示.下列有关说法中,不正确的是( )
已知:2Fe2++Br2═2Fe3++2Br-,2Fe3++2I-═2Fe2++I2.向FeI2、FeBr2的混合溶液中通入适量氯气,溶液中某些离子的物质的量变化如图所示.下列有关说法中,不正确的是( )| A. | 还原性:I->Fe2+>Br- | |
| B. | 原混合溶液中FeBr2的物质的量为6 mol | |
| C. | 当通入2 mol Cl2时,溶液中已发生的离子反应可表示为:2Fe2++2I-+2Cl2═2Fe3++I2+4Cl- | |
| D. | 原溶液中:n(Fe2+):n(I-):n(Br-)=2:1:3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 有关元素X、Y、Z、D、E的信息如下
有关元素X、Y、Z、D、E的信息如下| 元素 | 有关信息 |
| X | 元素主要化合价为-2,原子半径为0.074nm |
| Y | 所在主族序数与所在周期序数之差为4 |
| Z | 原子半径为0.102nm,核外最外层电子数是其电子层数的2倍,其单质在X的单质中燃烧,产生的气体通入品红中,品红褪色. |
| D | 最高价氧化物对应的水化物,是强电解质,能电离出电子数相等的阴、阳离子 |
| E | 单质是生活中常见金属,其制品在潮湿空气中易被腐蚀或损坏 |
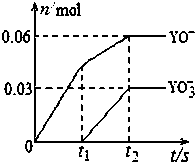
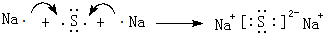 ,D2Z水溶液显碱性,用离子方程式表示其原因S2-+H2O?HS-+OH-
,D2Z水溶液显碱性,用离子方程式表示其原因S2-+H2O?HS-+OH-查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com