
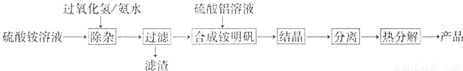
(12分)高纯氧化铝可用于制高压钠灯的陶瓷管。实验室制取高纯氧化铝的流程如下: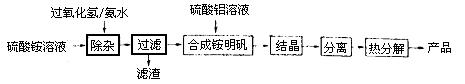
(1)“除杂”操作是加入适量过氧化氢,用氨水调节溶液的pH约为8.0,以除去硫酸铵溶液中的少量Fe2+。检验Fe2+是否除尽的实验操作是 。
(2)通常条件下,KSP[Fe(OH)3]=4.0×10-36,除杂后溶液中c(Fe3+)= 。
(3)配制硫酸铝溶液时,需用硫酸酸化,酸化的是目的是 。
(4)“结晶”操作中,母液经蒸发浓缩至溶液表面刚出现薄层的结晶为止,冷却结晶,得到铵明矾(含结晶水)。母液不能蒸干的原因是 。
(5)“分离”操作名称是 (填字母代号)
A.蒸馏 B.分液 C.过滤W ww.k s5u.co m
(6)测定铵明矾组成的方法是:
a.称取0.906g铵明矾样品,高温灼烧,得Al2O3残留固体0.1020g;
b. 称取0.4530g铵明矾样品,用适量蒸馏水溶解,再加入稍过量的BaCl2溶液,经陈化、过滤、灰化,得BaSO40.4659g;
c. 称取0.4530g样品,加入足量的NaOH溶液,加热,产生气体依次通过碱石灰和浓硫酸,浓硫酸增重0.0170g。
则铵明矾的化学式为 。
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
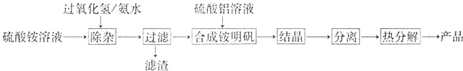
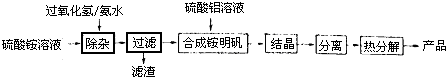
高纯氧化铝可用于制高压钠灯的陶瓷管。实验室制取高纯氧化铝的流程如下:
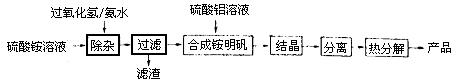
(1)“除杂”操作是加入适量过氧化氢,用氨水调节溶液的pH约为8.0,以除去硫酸铵溶液中的少量Fe2+。检验Fe2+是否除尽的实验操作是 。
(2)通常条件下,KSP[Fe(OH)3]=4.0×10-36,除杂后溶液中c(Fe3+)= 。
(3)配制硫酸铝溶液时,需用硫酸酸化,酸化的是目的是 。
(4)“结晶”操作中,母液经蒸发浓缩至溶液表面刚出现薄层的结晶为止,冷却结晶,得到铵明矾(含结晶水)。母液不能蒸干的原因是 。
(5)“分离”操作名称是 (填字母代号)
A.蒸馏 B.分液 C.过滤W ww.k s5u.co m
(6)测定铵明矾组成的方法是:
a.称取0.906g铵明矾样品,高温灼烧,得Al2O3残留固体0.1020g;
b. 称取0.4530g铵明矾样品,用适量蒸馏水溶解,再加入稍过量的BaCl2溶液,经陈化、过滤、灰化,得BaSO40.4659g;
c. 称取0.4530g样品,加入足量的NaOH溶液,加热,产生气体依次通过碱石灰和浓硫酸,浓硫酸增重0.0170g。
则铵明矾的化学式为 。
查看答案和解析>>
科目:高中化学 来源:2012年浙江省杭州市高考化学一模试卷(解析版) 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com