
| A. | 在羽毛球、网球等体育项目中做球拍的碳纤维材料是一种新型无机非金属材料 | |
| B. | 从海水中提取溴和镁都必须通过化学反应才能实现 | |
| C. | 聚乙烯塑料的老化是由于发生了加成反应 | |
| D. | 用饱和NH4Cl溶液可除去铁表面的锈斑 |
分析 A.碳纤维是一种含碳量在95%以上的高强度的新型纤维材料;
B.海水中的溴和镁均以化合态存在,提取溴和镁均需经过化学反应;
C.聚乙烯已经不存在双键;
D.饱和NH4Cl溶液中水解使溶液呈酸性.
解答 解:A.碳纤维是一种含碳量在95%以上的高强度的新型纤维材料,是一种新型的无机非金属材料,故A正确;
B.海水中的溴和镁均以化合态存在,提取溴和镁均需经过化学反应,故B正确;
C.聚乙烯已经不存在双键,不能发生加成反应,故C错误;
D.饱和NH4Cl溶液中水解使溶液呈酸性,铁表面锈斑的主要成分为铁的氧化物,可与其反应而除去,故D正确.
故选C.
点评 本题考查了无机非金属材料、海水的综合利用、聚乙烯的性质、盐的水解原理的应用,题目难度不大,注意基础知识的积累,侧重于考查学生的分析能力和对基础知识的应用能力.


科目:高中化学 来源: 题型:解答题
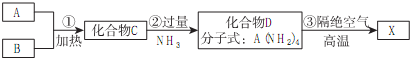

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
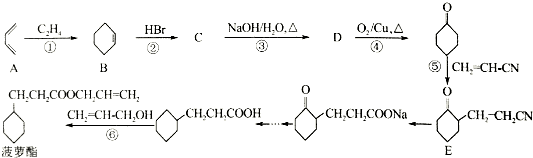
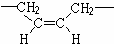 ,若顺丁橡胶的平均相对分子质量为540054,则平均聚合度为10001.
,若顺丁橡胶的平均相对分子质量为540054,则平均聚合度为10001.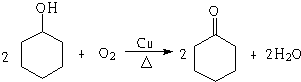 .
.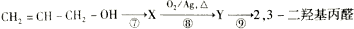
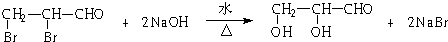 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
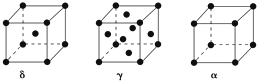
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硫酸亚铁溶液中加入用硫酸酸化的过氧化氢溶液:Fe2++2H++H2O2═Fe3++2H2O | |
| B. | 已知同温度下的溶解度:Zn(OH)2>ZnS,Na2S溶液与ZnCl2溶液混合:Zn2++S2-+2H2O═Zn(OH)2↓+H2S↑ | |
| C. | 0.01 mol•L-1NH4Al(SO4)2溶液与0.02 mol•L-1 Ba(OH)2溶液等体积混合:Al3++2SO42-+2Ba2++4OH-═2BaSO4↓+AlO2-+2H2O | |
| D. | 向KI-淀粉溶液中加入稀硫酸,在空气中放置一段时间后,溶液呈蓝色:4H++4I-+O2═2I2+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
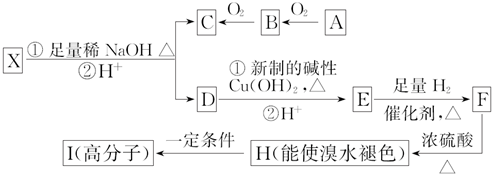
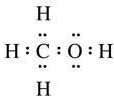 ;I的结构简式为
;I的结构简式为 .
.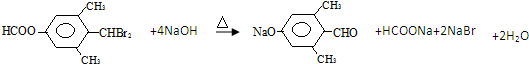 ;
; 任意一种.
任意一种.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
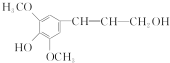
| A. | 芥子醇的分子式为C11H14O4 | |
| B. | 芥子醇分子中所有碳原子可能在同一平面上 | |
| C. | 1 mol该化合物在一定条件下最多可与2molNaOH反应 | |
| D. | 芥子醇在一定条件下能发生氧化、取代、加成、酯化反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
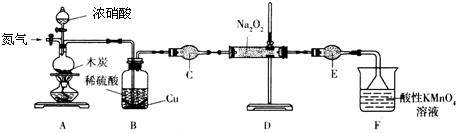
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com