
| A. | HCl | B. | BaCl2 | C. | AgNO3 | D. | NaOH |
分析 四种盐溶液的阳离子各不相同,可从阳离子鉴别的角度分析,鉴别阳离子,可加入碱,结合氢氧化铝的两性以及氨气的刺激性气味等角度判断.
解答 解:A.加入盐酸都不反应,不能鉴别,故A错误;
B.加入氯化钡,只能鉴别硫酸铝,故B错误;
C.加入硝酸银,NaCl、MgCl2、Al2(SO4)3都生成沉淀,不能鉴别,
D.加入氢氧化钠,NaCl无现象、MgCl2生成白色沉淀,Al2(SO4)3先生成白色沉淀,后溶解,NH4NO3生成刺激性气体,现象各不相同,可鉴别,故D正确.
故选D.
点评 本题考查物质的检验和鉴别,为高考常见题型和高频考点,侧重于学生的分析能力和实验能力的考查,注意把握物质的性质的异同,难度不大.


科目:高中化学 来源: 题型:选择题
| A. | ① | B. | ③ | C. | ②③ | D. | ①④ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
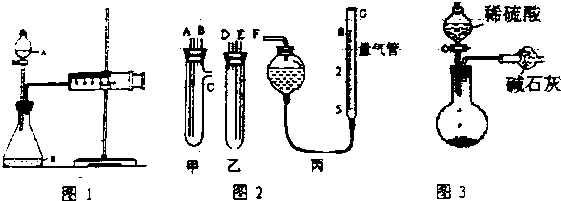
查看答案和解析>>
科目:高中化学 来源: 题型:解答题


查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 都是混合物 | B. | 都含有氧元素 | ||
| C. | 资源充足,可以任意使用 | D. | 大部分物质相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com