
| 编号 | 现象 | 离方程式 |
| ① | ||
| ② | ||
| ③ |
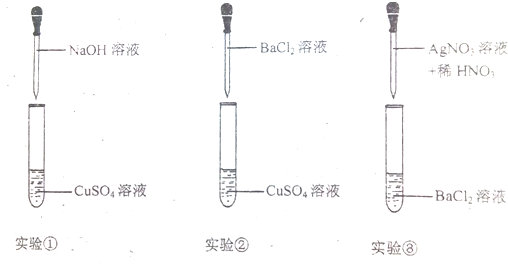
分析 ①硫酸铜和NaOH反应生成Cu(OH)2蓝色沉淀;
②硫酸铜和氯化钡反应生成白色BaSO4沉淀;
③氯化钡和硝酸银反应生成白色AgCl沉淀.
解答 解:①硫酸铜和NaOH反应生成Cu(OH)2蓝色沉淀,看到的现象是有蓝色沉淀产生,离子方程式为Cu2++2OH-=Cu(OH)2↓;
②硫酸铜和氯化钡反应生成白色BaSO4沉淀,看到的现象是有白色沉淀生成,离子方程式为Ba2++SO42-=BaSO4↓;
③氯化钡和硝酸银反应生成白色AgCl沉淀,看到的现象是有白色沉淀生成,离子方程式为Ag++Cl-=AgCl↓,
故答案为:
| 编号 | 现象 | 离子方程式 |
| ① | 有蓝色沉淀产生 | Cu2++2OH-=Cu(OH)2↓ |
| ② | 有白色沉淀产生 | Ba2++SO42-=BaSO4↓ |
| ③ | 有白色沉淀产生 | Ag++Cl-=AgCl↓ |
点评 本题考查离子方程式的书写,为高频考点,明确物质之间发生的反应及离子方程式书写分子是解本题关键,知道常见物质颜色,题目难度不大.


科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用分液的方法分离煤油和汽油 | |
| B. | 加稀盐酸后过滤,除去混在铜粉中的少量镁粉 | |
| C. | 用溶解、过滤的方法分离K2MnO4和KMnO4固体的混合物 | |
| D. | 将氧气和氢气的混合气体通过灼热的氧化铜,以除去其中的氢气 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com