
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | |||
| 4 | ⑧ | ⑨ |
分析 (1)由元素在周期表中的位置可知,①是C、②是O、③是Na、④是Mg、⑤是Al、⑥是Cl、⑦是Ar、⑧是K、⑨是Br,其中稀有气体化学性质最不活泼;
(2)金属性越强,最高价氧化物对应水化物的碱性越强;氢氧化钠与氢氧化铝反应生成偏铝酸钠和水;
(3)同周期自左而右原子半径减小,同主族自上而下原子半径增大;
(4)⑧元素与⑥元素形成的化合物KCl,钾元素的焰色反应为紫色.
解答 解:(1)由元素在周期表中的位置可知,①是C、②是O、③是Na、④是Mg、⑤是Al、⑥是Cl、⑦是Ar、⑧是K、⑨是Br,其中稀有气体Ar化学性质最不活泼,
故答案为:C;O; Na; Mg;Al;Cl;Ar; K; Br; Ar;
(2)非金属性Na>Mg>Al,金属性越强,最高价氧化物对应水化物的碱性越强,故NaOH的碱性最强;氢氧化钠与氢氧化铝反应生成偏铝酸钠和水,反应方程式为:Al(OH)3+NaOH=NaAlO2+2H2O,
故答案为:NaOH;Al(OH)3+NaOH=NaAlO2+2H2O;
(3)同周期自左而右原子半径减小,同主族自上而下原子半径增大,故原子半径:Na>C>O,
故答案为:Na>C>O;
(4)⑧元素与⑥元素形成的化合物是KCl,钾元素的焰色反应为紫色,观察时需要透过透过蓝色钴玻璃,
故答案为:紫;透过蓝色钴玻璃.
点评 本题考查周期表和周期律的应用,为高频考点,侧重于分析与应用能力的考查,把握元素的位置和性质、元素周期律等为解答该题的关键,题目难度不大.


科目:高中化学 来源: 题型:解答题
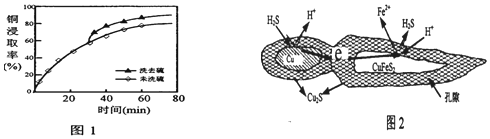
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
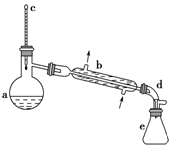 醇脱水是合成烯烃的常用方法,实验室合成环己烯的反应和实验装置如图:
醇脱水是合成烯烃的常用方法,实验室合成环己烯的反应和实验装置如图: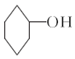 $→_{△}^{浓硫酸}$
$→_{△}^{浓硫酸}$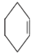 +H2O,
+H2O,| 相对分子质量 | 密度/(g•cm-3) | 沸点/℃ | 溶解性 | |
| 环己醇 | 100 | 0.961 8 | 161 | 微溶于水 |
| 环己烯 | 82 | 0.810 2 | 83 | 难溶于水 |
 ,生成该物质的反应类型是取代反应
,生成该物质的反应类型是取代反应查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | X可能呈酸性 | B. | X溶液可能呈中性 | C. | Y溶液可能呈中性 | D. | Y溶液一定呈中性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 弱酸 | HCOOH | HCN | H2S |
| 电离平衡常数(25℃) | Ka=1.8×10-4 | Ka=4.9×10-10 | Ka1=1.3×10-7 Ka2=7.1×10-15 |
| A. | 恰好中和等体积、等pH的HCOOH和HCN消耗NaOH的量前者大于后者 | |
| B. | HCOO-、CN-、HS-在溶液中不可以大量共存 | |
| C. | NaHS溶液中加入适量KOH后:c(Na+)═c(H2S)+c(HS-)+2C(S2-) | |
| D. | 等体积、等浓度的HCOONa和NaCN两溶液中所含离子总数目HCOONa大于NaCN |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 18 g D2O和18 g H2O中含有的质子数均为10 NA | |
| B. | 22.4 LC02中含有共价键数目4 NA | |
| C. | 若H2O2分解产生成0.1mol氧气转移的电子数为0.2 NA | |
| D. | 同温、同压同体积的CO和NO含有的电子数相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 金刚石网状结构中,由共价键形成的碳原子环中,最小的环上有6个碳原子 | |
| B. | 12g石墨中含有σ键的个数为2NA (NA表示阿伏伽德罗常数) | |
| C. | 氯化铯晶体中,每个Cs+周围紧邻8个Cl- | |
| D. | 干冰晶体中,每个CO2分子周围紧邻12个CO2分子 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
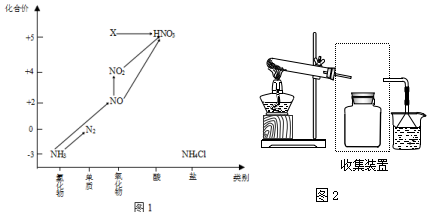
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com