
分析 依据向容积为2L的密闭容器中充入0.4molSO2、0.18molO2和1.2molSO3的混合气体,依据平衡常数的计算方法计算出浓度商,然后根据计算结果与化学平衡常数比较来判断是否达到平衡状态,若平衡后从体系中移走SO3,是减少生成物的浓度,根据化学平衡移动原理可知平衡正向进行.
解答 解:2L的密闭容器中充入0.4molSO2、0.18molO2和1.2molSO3的混合气体,各气体的浓度为:c(SO2)=$\frac{0.4mol}{2L}$=0.2mol/L、c(O2)=$\frac{0.18mol}{2L}$=0.09mol/L、c(SO3)=$\frac{1.2mol}{2L}$=0.6mol/L,此时的浓度商为:Qc=$\frac{{c}^{2}(S{O}_{3})}{{c}^{2}(S{O}_{2})c({O}_{2})}$=$\frac{(0.6mol/L)^{2}}{(0.2mol/L)^{2}×0.09mol/L}$=100<K=600,反应正向移动,说明该反应没有达到平衡状态;若平衡后从体系中移走SO3,减少生成物的浓度,则平衡向着正反应向移动,
故答案为:否,正反应.
点评 本题考查化学平衡常数分析应用、反应进行方向判断的方法等知识,化学平衡移动原理的理解应用,平衡常数和浓度商的计算比较是解题关键,题目难度不大.


科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
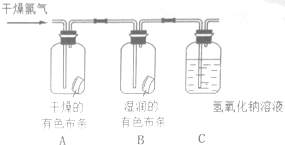 为了验证氯气的有关行政,某同学设计了如下的实验.
为了验证氯气的有关行政,某同学设计了如下的实验.查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
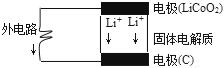 锂电池的构造如图所示,电池内部“→”表示放电时Li*的迁移方向,电池总反应可表示为:Li1-xCoO2+LixC$?_{放电}^{充电}$LiCoO2+6C,下列说法错误的是( )
锂电池的构造如图所示,电池内部“→”表示放电时Li*的迁移方向,电池总反应可表示为:Li1-xCoO2+LixC$?_{放电}^{充电}$LiCoO2+6C,下列说法错误的是( )| A. | 该电池的负极为LiCoO2 | |
| B. | 电池中的固体电解质可以是熔融的氯化钠、干冰等 | |
| C. | 充电时的阴极反应:Li1-xCoO2+xLi++xe-═LiCoO2 | |
| D. | 外电路上的“→”表示放电时的电子流向 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 中含有
中含有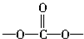 结构.
结构.| A. | ②⑤ | B. | ②④⑥ | C. | ①②③⑥ | D. | ②④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 钠 | Na2CO3 | 金刚石 | 石墨 | |
| 熔点(℃) | 97.8 | 851 | 3550 | 3850 |
| 沸点(℃) | 882.9 | 1850(分解产生CO2) | ---- | 4250 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com