
���� ��1�����A��B��C�������壬�ڼ�ѹ��ƽ�����淴Ӧ�����ƶ�����Сѹǿƽ���������������ķ����ƶ���
��2��C�����壬����x+y=z���ڼ�ѹʱ��ѧƽ��ɷ����ƶ���A��B�������壬����ѹǿ��ƽ�������������С�ķ����ƶ���
��3��B��C�����壬������A���ʵ�����ƽ�ⲻ�ƶ���˵��A����������ƽ���ƶ��أ���A�Ƿ���̬���ʣ�
��4�������¶ȣ�ƽ�������ȷ����ƶ���
��� �⣺��1����Сѹǿƽ���������������ķ����ƶ������A��B��C�������壬�ڼ�ѹ��ƽ�����淴Ӧ�����ƶ���˵���淴Ӧ�������������x+y��z���ʴ�Ϊ��x+y��z��
��2��C�����壬����x+y=z����Ӧǰ��������������ڼ�ѹʱ��ѧƽ�������������С�ķ����ƶ���A��B�������壬����ѹǿ��ƽ�����淴Ӧ�����ƶ����ʴ�Ϊ���淴Ӧ��
��3��B��C�����壬������A���ʵ�����ƽ�ⲻ�ƶ���˵��A����������ƽ���ƶ��أ���A�Ƿ���̬���ʣ��ʴ�Ϊ��������
��4�������¶ȣ�ƽ�������ȷ����ƶ��������Ⱥ�A�İٷֺ������ӣ�˵��ƽ�������ƶ���������Ӧ�Ƿ��ȷ�Ӧ���ʴ�Ϊ���ţ�
���� ���⿼�黯ѧƽ��Ӱ�����أ�Ϊ��Ƶ���㣬��ȷ�¶ȡ�ѹǿ��Ũ�ȶԻ�ѧƽ��Ӱ��ԭ���ǽⱾ��ؼ���ע�����Ӱ���������÷�Χ����Ŀ�ѶȲ���


 ��ĩ�����ϵ�д�
��ĩ�����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 2.2mol | B�� | 1mol | C�� | 1.6mol | D�� | 2mol |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ̼-14���أ�${\;}_8^{14}C$ | B�� | Ca2+�Ľṹʾ��ͼΪ  | ||
| C�� | �����ĵ���ʽ | D�� | HCIO�ĽṹʽΪH-Cl-O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ˮ���� | B�� | ��Na0H��Һ����� | C�� | ��Na2SO4��Һ | D�� | ֱ�ӹ۲� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ̼��������Һ����������������Һ��ϣ�2HCO3-+Ca2++2OH-�TCaCO3��+2H2O+CO32- | |
| B�� | ��ʯī���缫�������ͭ��Һ��2Cu2++2H2O$\frac{\underline{\;���\;}}{\;}$2Cu+O2��+4H+ | |
| C�� | ��FeBr2��Һ��ͨ�������Cl2��2Br-+2Fe2++2Cl2�TBr2+2Fe3++4Cl- | |
| D�� | ����������Һ�м�������İ�ˮ��Al3++4NH3•H2O�TAlO2-+4NH4++2H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
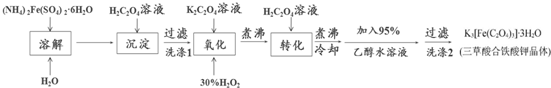
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
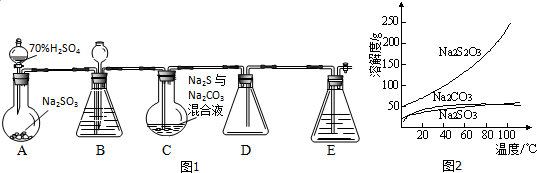
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �״� | B�� | ��Ȳ | C�� | �Ҵ� | D�� | ��ȩ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
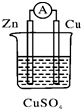
| A�� | ������п�缫ͨ������������ͭ�缫 | |
| B�� | п�缫������ԭ��Ӧ��ͭ�缫����������Ӧ | |
| C�� | ����13 g Zn�ܽ�ʱ�����·�о���0.4 mol����ͨ�� | |
| D�� | ͭ�缫�������������ĵ缫��ӦΪ2H++2e-�TH2�� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com