
| A. | 90% | B. | 80% | C. | 45% | D. | 10% |
分析 将1体积A(g)和3体积B(g)混合,设物质的量分别为1mol、3mol,
设A的转化率为x,气体的密度比与物质的量之比成反比,
对于反应:2A(g)+B(g)?2C(g),
开始(mol):1 3 0
变化(mol):1×x 0.5x x
平衡(mol) 1-x 3-0.5x x
根据密度之比列式为:(1-x+3-0.5x+x):(1+3)=9:10,计算x,可计算A的转化率.
解答 解:将1体积A(g)和3体积B(g)混合,设物质的量分别为1mol、3mol,
设A的转化率为x,气体的密度比与物质的量之比成反比,
对于反应:2A(g)+B(g)?2C(g),
开始(mol):1 3 0
变化(mol):1×x 0.5x x
平衡(mol) 1-x 3-0.5x x
根据密度之比列式为:(1-x+3-0.5x+x):(1+3)=9:10,
解得:x=0.8,
则A转化率为$\frac{0.8}{1}×100%$=80%,
故选B.
点评 本题考查了化学平衡的计算应用,为高频考点,题目难度中等,明确三段式在化学平衡计算中的应用方法,试题培养了学生的分析能力及化学计算能力.


科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:实验题
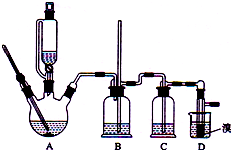 实验室制备1,2-二溴乙烷的反应原理如下:
实验室制备1,2-二溴乙烷的反应原理如下:| 乙醇 | 1,2-二溴乙烷 | 乙醚 | |
| 状态 | 无色液体 | 无色液体 | 无色液体 |
| 密度/g•cm-3 | 0.79 | 2.2 | 0.71 |
| 沸点/℃ | 78.5 | 132 | 34.6 |
| 熔点/℃ | 一l30 | 9 | -1l6 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 1.0MPa | 2.0MPa | 3.0MPa | |
| 810℃ | 54.0% | a | b |
| 915℃ | c | 75.0% | d |
| 1000℃ | e | f | 83.0% |
| A. | 1个 | B. | 2个 | C. | 3个 | D. | 4个 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 时间/s | 20 | 40 | 60 | 80 | 100 |
| c(NO2 )/(mol/L) | 0.12 | 0.20 | 0.26 | 0.30 | 0.30 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2v正(B)=v逆(C) | B. | 该体系的密度都不随时间变化 | ||
| C. | 1molA断裂,同时1molC也断裂 | D. | 该体系的温度不随时间而变化 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com