
【题目】(1)![]() 碳与适量水蒸气反应生成CO和H2,需吸收
碳与适量水蒸气反应生成CO和H2,需吸收![]() 热量,此反应的热化学方程式为_________________
热量,此反应的热化学方程式为_________________
(2)已知![]() ;
;![]()
![]() ;
;![]()
![]() ;
;![]()
常温下,取体积比4:1的甲烷和氢气的混合气体![]() (标准状况下),经完全燃烧后恢复至室温,则放出的热量为___________
(标准状况下),经完全燃烧后恢复至室温,则放出的热量为___________
【答案】C(s) + H2O(g) = CO(g) + H2(g) ΔH= + 131.28 kJ·mol-1 0.4Q1 + 0.05 molQ3
【解析】
⑴1 g碳与适量水蒸气反应生成CO和H2,需吸收10.94KJ热量,则1 mol碳即12 g与适量水蒸气反应生成CO和H2,需吸收131.28 4KJ热量,此反应的热化学方程式为
C(s) + H2O(g) = CO(g) + H2(g) ΔH= + 131.28 kJ·mol-1
⑵常温下,取体积比4:1的甲烷和氢气的混合气体11.2 L即物质的量为0.5 mol,甲烷物质的量为0.4 mol,氢气的物质的量为0.1 mol,根据方程式①③,经完全燃烧后恢复至室温,则放出的热量为0.4Q1 + 0.05 molQ3。
故答案为0.4Q1 + 0.05 molQ3。


科目:高中化学 来源: 题型:
【题目】有下列分子或离子:①CS2, ②PCl3, ③H2S, ④CH2O, ⑤H3O+, ⑥NH![]() ,⑦BF3,⑧SO2。
,⑦BF3,⑧SO2。
(1)粒子的立体构型为直线形的有____________ (填序号,下同);
(2)粒子的立体构型为V形的有______________;
(3)粒子的立体构型为平面三角形的有______________;
(4)粒子的立体构型为三角锥形的有______________;
(5)粒子的立体构型为正四面体形的有______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2A1+MoO3![]() Mo+Al2O3用于制备金属钼(Mo)。下列说法正确的是
Mo+Al2O3用于制备金属钼(Mo)。下列说法正确的是
A.Al得电子B.Al2O3 是氧化剂
C.MoO3 发生还原反应D.每生成1molMo有3mol电子转移
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知2HI(g)H2(g) +I2(g), 443℃时IL密闭容器中充入1 mol HI,体系中c(HI)与反应时间t的关系如图所示。下列说法正确的是
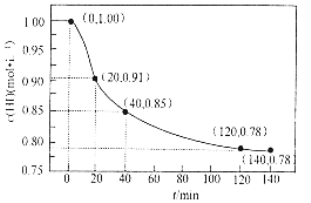
A.0~20 min内,v(H2) = 0.0045mol·L-1·min-1B.升高温度,HI会完全分解
C.40 min时,c(H2) = 0.075mol·L-1D.120 min反应达到最大限度,此时HI的转化率为78%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如果阿伏加德罗常数的值为NA。下列说法正确的是( )
A.![]() 与
与![]() 所含的分子数一定相等
所含的分子数一定相等
B.将![]() 钠用铝箱包裹并刺小孔,与足量水充分反应生成H2分子数为
钠用铝箱包裹并刺小孔,与足量水充分反应生成H2分子数为![]()
C.![]() 与足量水反应转移
与足量水反应转移![]() 电子
电子
D.高温下,![]() 与足量水蒸气完全反应,转移的电子数为
与足量水蒸气完全反应,转移的电子数为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学是研究物质的组成,结构,性质以及变化规律的一门以实验为基础的学科,在给定条件下,下列物质间转化均能实现的一组是( )
(1)![]()
(2)![]()
(3)![]()
(4)![]()
A.(1)(2)B.(2)(3)C.(2)(4)D.(3)(4)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质的分子中既有σ键,又有π键,并含有非极性键的是( )
①H2O2 ②N2 ③H2O ④HCl ⑤C2H4 ⑥C2H2
A. ②⑤⑥ B. ①②⑤⑥
C. ②④⑥ D. ②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有含NaCl、Na2SO4和NaNO3的混合物,选择适当的试剂将其转化为相应的沉淀或固体,从而实现Cl-、SO42-、和NO3-的相互分离。相应的实验过程可用下图表示:

请回答下列问题:
(1)写出实验流程中下列物质的化学式:
试剂X :______________ 沉淀A:______________ 沉淀B:________________。
(2)上述实验流程中加入过量的Na2CO3的目的是____________________________。
(3)按此实验方案得到的溶液3中肯定含有__________(填化学式)杂质。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚硝酸钠(NaNO2)在纤维纺织品的染色和漂白、照相、生产橡胶、制药等领域有广泛应用,也常用于鱼类、肉类等食品的染色和防腐。但因其有毒,所以在食品行业中的用量有严格限制。现用下图所示仪器(夹持装置已省略)及药品,探究亚硝酸钠与硫酸反应及气体产物的成分。
已知:①NO+NO2+2OH-===2NO2-+H2O;
②气体液化的温度:NO2为21 ℃,NO为-152 ℃。
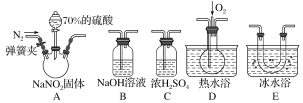
(1)为了检验装置A中生成的气体产物,仪器的连接顺序(按左→右连接)为A、C、________、________、________。
(2)反应前应打开弹簧夹,先通入一段时间氮气,排除装置中的空气,目的是________________________________________________________________________。
(3)在关闭弹簧夹、打开分液漏斗活塞、滴入70%硫酸后,A中产生红棕色气体。
①确认A中产生的气体含有NO,依据的现象是________________________。
②装置E的作用是_________________________________________________。
(4)如果向D中通入过量O2,则装置B中发生反应的化学方程式为___________。
(5)通过上述实验探究过程,可得出装置A中反应的化学方程式是__________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com