
(A)常温同浓度(mol![]() )NaOH溶液的电离度和HY
)NaOH溶液的电离度和HY![]() 的电离度相比较前者略大于后者
的电离度相比较前者略大于后者
(B)HY![]() 在水解时为:HY
在水解时为:HY![]() +H
+H![]() O
O![]() Y
Y![]() +H
+H![]() O
O![]()
(C)该盐溶液中离子浓度的顺序是:[Na![]() ] > [HY
] > [HY![]() ] > [OH
] > [OH![]() ] > [H
] > [H![]() ]
]
(D)该盐溶液中离子浓度的顺序是:[Na![]() ] > [Y
] > [Y![]() ] > [HY
] > [HY![]() ] > [OH
] > [OH![]() ] > [H
] > [H![]() ]
]
| 在NaHY在水溶液中,由于HY A中,氢氧化钠是强电解质,其在水溶液中应是全部电离,要说电离度可以认为是100%。该酸的酸式根既能电离又能水解,而且酸式根的电离度小于HY B中,在书写水解的离子方程式时,由于思维定势,见到反应物中有弱电解质离子和水,就认为一定发生水解反应,因此误选了B选项。实际上反应物中有水参与,并不表示一定就是发生水解,还存在一类属于电离的变化,即水和电离产生的氢离子形成水合氢离子(又称卉离子),所以在分析这类问题时,不仅要看反应物,还得分析生成物,这样才能减少判断失误。 D中,在分析离子浓度大小时,不管是弱电解质电离也好,还是弱电解质对应离子要发生水解也好,在没有其它信息给予时,其发生变化的量将远远小于平衡中剩余的量,因此Y
|


 53随堂测系列答案
53随堂测系列答案科目:高中化学 来源:2013届山东省济南世纪英华实验学校高三上学期期末考试化学试卷(带解析) 题型:单选题
某酸的酸式盐NaHY在水溶液中,HY-的电离程度小于HY-的水解程度。有关的叙述正确的是
| A.H2Y的电离方程式为:H2Y |
| B.在该酸式盐溶液中:[Na+]>[Y2-]>[HY-]>[OH-]>[H+] |
C.HY-的水解方程式:HY-+H2O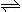 H3O++Y2- H3O++Y2- |
| D.在该酸式盐溶液中:[Na+]>[HY-]>[OH-]>[Y2-]>[H+] |
查看答案和解析>>
科目:高中化学 来源:2012-2013学年山东省高三上学期期末考试化学试卷(解析版) 题型:选择题
某酸的酸式盐NaHY在水溶液中,HY-的电离程度小于HY-的水解程度。有关的叙述正确的是
A.H2Y的电离方程式为:H2Y
B.在该酸式盐溶液中:[Na+]>[Y2-]>[HY-]>[OH-]>[H+]
C.HY-的水解方程式:HY-+H2O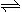 H3O++Y2-
H3O++Y2-
D.在该酸式盐溶液中:[Na+]>[HY-]>[OH-]>[Y2-]>[H+]
查看答案和解析>>
科目:高中化学 来源:2010-2011学年山东省高三上学期第三次质量检测化学试卷 题型:选择题
下列选项中正确的是
A. 1L0.5mol·L-1稀硫酸与1L1mol·L-1氢氧化钠溶液反应放出57.3kJ的热量:
H2SO4(aq) +2NaOH(aq) = Na2SO4(aq) +2H2O(1);△ H = -57.3 kJ· mol-1
B. 某酸的酸式盐NaHY水溶液显碱性,则H2Y 2H++Y2—
2H++Y2—
C. 纯碱溶液显碱性的原因用离子方程式可表示为:CO32—+2H2O H2CO3+2OH—
H2CO3+2OH—
D.以惰性电极电解KCl溶液的离子方程式为:2Cl-+2H2O  H2↑+2OH-+Cl2↑
H2↑+2OH-+Cl2↑
查看答案和解析>>
科目:高中化学 来源:2013届辽宁省东北育才学校高二上学期期中考试化学试卷 题型:选择题
某酸的酸式盐NaHY的水溶液中,HY-的电离程度小于HY-的水解程度,有关叙述中正确的是( )
A、H2Y在电离时为:H2Y+H2O
 HY-+H3O+
HY-+H3O+
B、在该盐的溶液中,离子浓度为:
c(Na+)>c(Y2-)>c(HY-)>c(OH-)>c(H+)
C、在该盐的溶液中,离子浓度为:
c(Na+)>c(HY-)>c(Y2-)>c(OH-)>c(H+)
D、HY-的水解方程式为:HY-+H2O
 H3O++Y2-
H3O++Y2-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com