
| 1 |
| 2 |


科目:高中化学 来源: 题型:
A、当x≤
| ||
| B、当x≥n时,反应的离子方程式为:2Fe2++2I-+2Cl2→2Fe3++I2+4Cl- | ||
| C、当Fe2+和I-都被氧化时,x与n的关系为x>n | ||
| D、当x=n时,反应后氧化产物的物质的量为n mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、N5+常温下会剧烈爆炸,体积急剧膨胀,放出大量的热 |
| B、N60的发现开辟了能源世界的新天地,将来可能成为很好的火箭燃料 |
| C、N2、N3、N5、N5+、N60互为同素异形体 |
| D、含N5+的化合物中既有离子键又有共价键 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 溶质 | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN | C6H5ONa |
| pH | 8.8 | 9.7 | 11.6 | 10.3 | 11.1 | 11.3 |
| A、少量二氧化碳通入NaClO溶液中:2NaClO+CO2+H2O→Na2CO3+2HClO |
| B、过量的 HCN滴入碳酸钠溶液中 HCN+Na2CO3→NaCN+NaHCO3 |
| C、结合质子能力由强到弱的顺序为:CO32->CN->HCO3->CH3COO- |
| D、常温下电离常数:Ki2(H2CO3)>Ki(C6H5OH)>Ki(HCN) |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
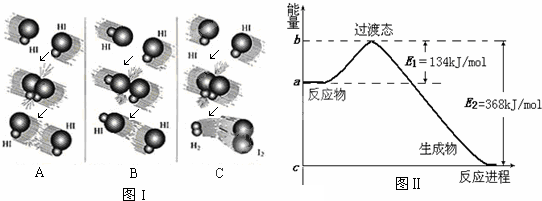
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

| n(SO3) |
| n(SO2) |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com