
(1)相同物质的量的O2和O3的质量比为_________;所含氧原子的个数比为______________。
(2)2.5 mol Ba(OH)2中含有_________个OH—,2.5 mol Ba(OH)2的质量是____________g。
(3)在标准状况下,1.7 g氨气所占的体积约为__________L,它与标准状况________L硫化氢含有相同数目的氢原子。
(4)某气态氧化物化学式为RO2,在标准状况下,1.28 g该氧化物的体积为448 mL,则该氧化物的摩尔质量为________________。
(5)同温同压下,SO2与氦气的密度之比为________,若质量相同,两种气体的体积比为_____。
科目:高中化学 来源:2015-2016学年辽宁省高二下期初摸底化学卷(解析版) 题型:填空题
巴伊亚祖母绿号称是世界上最大的祖母绿矿石,重380余公斤,含有约18万克拉的祖母绿宝石,价值约4亿美元。祖母绿的元素组成是O、Si、Al、Be,化学式为Be3Al2Si6O18 。
(1)基态Al原子中,电子占据的最高能级的符号是 ,该能级具有的原子轨道数为 。
(2)在500~600℃气相中,氯化铍以二聚体Be2Cl4的形式存在(如图),在1000℃,氯化铍则以BeCl2形式存在。在BeCl2分子中,Be的杂化方式为 ,二聚体Be2Cl4中Be的杂化方式为 ,1mol Be2Cl4中含有 mol配位键。

(3)氢化铝锂(LiAlH4)是有机合成中的一种重要还原剂,可以将羧基还原为羟基,如可将乙酸还原为乙醇,乙酸和乙醇的熔沸点数据如下:
| 乙酸 | 乙醇 |
熔点/℃ | 16.6 | -114.3 |
沸点/℃ | 117.9 | 78.4 |
乙酸分子中σ键与π键数目之比为 ,由表格中的数据知,乙酸的熔沸点均比乙醇高,原因是 。
(4)图示为Be与O形成的氧化物的立方晶胞结构,已知氧化铍的密度ρ=3.00g/cm3,则晶胞参数a= nm。

查看答案和解析>>
科目:高中化学 来源:2015-2016学年内蒙古高一上第一次月考化学试卷(解析版) 题型:选择题
在1.01×105Pa,20℃时,下列气体各2.8L,其质量最大的是( )
A.N2 B.Cl2 C.NH3 D.SO2
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖北省高二上开学考试化学试卷(解析版) 题型:选择题
室温时,下列溶液等体积混合后pH一定小于7的是( )
A. pH=3的盐酸和pH=11的氨水 B. pH=3的盐酸和pH=11的氢氧化钡溶液
C. pH=3的硫酸和pH=11的氨水 D. pH=3的醋酸和pH=11的氢氧化钡溶液
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖北省高二上开学考试化学试卷(解析版) 题型:选择题
pH均为5的NH4Cl溶液和稀盐酸中,由水电离出的H+浓度比较( )
A.一样大 B.前者大 C.后者大 D.无法判断
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖北沙市高一上第一次双周练化学卷(解析版) 题型:实验题
(1)下列关于实验的叙述中正确的有__________。
A.实验时应节约药品,实验剩余的药品应放回原试剂瓶 |
B.不慎碰翻燃着的酒精灯使酒精在桌面上燃烧起来,应立即用湿抹布灭火 |
C.使用分液漏斗前要检查其是否漏水 |
D.用托盘天平称量物质质量时,物品应置于右盘 |
E.可燃性气体点燃前一定要验纯
F.不慎将酸沾到皮肤或衣物上,应立即用浓NaOH溶液清洗
(2)下图是中学化学中常用于混合物的分离和提纯的装置,请根据装置回答问题:
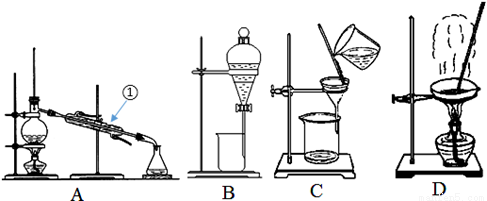
①从氯化钾溶液中得到氯化钾固体,选择装置 (填代表装置图的字母,下同);
分离CCl4(沸点为76.75℃)和甲苯(沸点为110.6℃)的液体混合物,选择装置__________,该分离方法的名称为______________。
②从碘水中分离出I2,选择装置__________,该分离方法的名称为__________,若将碘水和CCl4注入分液漏斗中充分振荡并静置后,碘主要溶解在 (填“上层”或“下层”)液体中,该层溶液颜色为__________。
③装置A中①的名称是__________,进水的方向是从___________(填“上”或“下”)口进水。装置B在分液时为使液体顺利下滴,应进行的具体操作 。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖北沙市高一上第一次双周练化学卷(解析版) 题型:选择题
用NA表示阿伏加德罗常数,下列叙述正确的是
A.常温常压下,4g H2含有的分子数为 2NA
B.8g H2O在标准状况下的体积是22.4L
C.2.3g金属钠变为钠离子时失去的电子数为NA
D.17g氨气所含电子数目为8NA
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖北沙市高二上第一次双周练化学卷(解析版) 题型:填空题
回答下列问题:
(1)已知下列反应:SO2 (g)+2OH–(aq) =SO32–(aq)+H2O(l) ΔH1;
ClO–(aq)+SO32–(aq)=SO42–(aq)+Cl–(aq) ΔH2;
CaSO4(s)=Ca2+(aq)+SO42–(aq) ΔH3。
则反应SO2(g)+Ca2+(aq)+ClO–(aq)+2OH–(aq)=CaSO4(s)+H2O(l)+Cl–(aq)的ΔH=______________。(用ΔH1、ΔH2、ΔH3表示)
(2)合成气(CO和H2为主的混合气体)不但是重要的燃料也是重要的化工原料,制备合成气的方法有多种,用甲烷制备合成气的反应为:①2CH4(g)+O2(g)=2CO(g)+4H2(g) ΔH1=-72 kJ·mol﹣1;
②CH4(g)+H2O(g)=CO(g)+3H2(g) ΔH2=+216 kJ·mol﹣1。现 有1 mol由H2O(g)与O2组成的混合气,且O2的体积分数为x,将此混合气与足量CH4充分反应。
有1 mol由H2O(g)与O2组成的混合气,且O2的体积分数为x,将此混合气与足量CH4充分反应。
若x=0.2时,反应①放出的能量为________kJ;
若x=_________时,反应①与②放出(或吸收)的总能量为0。
(3)一定条件,在水溶液中1 mol Cl-和1 mol ClOx(x=1,2,3,4)的能量(kJ)相对大小如图所示。

①D是________(填离子符号)。
②B→A+C反应的热化学方程式为_______________(用离子符号表示)。
查看答案和解析>>
科目:高中化学 来源:2016-2017年黑龙江佳木斯一中高一上9.10周练化学卷(解析版) 题型:选择题
用NA表示阿伏加德罗常数,下列叙述正确的是( )
A.标准状况下,22.4L苯含有的分子数为1NA
B.常温常压下,1.06gNa2CO3含有的Na+离子数为0.01NA
C.2.4g金属镁变成镁离子时失去的电子数为0.1NA
D.常温常压下,80gSO2含有的氧原子数为2.5NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com