
【题目】下图是研究铁钉腐蚀的装置图,下列说法不正确的是
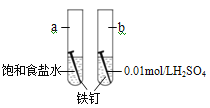
A. 铁钉在两处的腐蚀速率:a < b
B. a、b两处铁钉中碳均正极
C. a、b两处铁钉中的铁均失电子被氧化
D. a、b两处的正极反应式均为O2+4e-+4H+===2H2O
【答案】D
【解析】
试题a中电解质溶液显中性,为铁钉的吸氧腐蚀,b中电解质溶液为稀硫酸,显酸性为析氢腐蚀;
A、硫酸中氢离子浓度较大,电池反应较快,饱和食盐水中氧气的浓度较小,电池反应较慢;
B、a、b中C为原电池的正极;
C、a、b中Fe失电子为原电池的负极;
D、a中正极上氧气的得电子,b中正极上氢离子得电子.
解:a中电解质溶液显中性,为铁钉的吸氧腐蚀,b中电解质溶液为稀硫酸,显酸性为析氢腐蚀;
A、硫酸中氢离子浓度较大,电池反应较快,饱和食盐水中氧气的浓度较小,电池反应较慢,所以ab在两处的腐蚀速率a<b,故A正确;
B、a中C为原电池的正极,正极上氧气得电子,b中C为原电池的正极,正极上氢离子得电子,故B正确;
C、原电池中失电子的一极为负极,a、b中Fe失电子为原电池的负极,故C正确;
D、a中正极上氧气得电子,其电极反应式为O2+4e﹣+2H2O═4OH﹣,b中正极上氢离子得电子,其电极反应式为2H++2e﹣=H2↑,故D错误;
故选D.


科目:高中化学 来源: 题型:
【题目】NA表示阿伏加德罗常数的值。俗名为“臭碱”的硫化钠广泛应用于冶金染料、皮革、电镀等工业。硫化钠的一种制备方法是Na2SO4+2C![]() Na2S+2CO2↑。下列有关说法正确的是
Na2S+2CO2↑。下列有关说法正确的是
A. 1mol/LNa2SO4溶液中含氧原子的数目一定大于4NA
B. 1L0.1mol/LNa2S溶液中含阴离子的数目小于0.1NA
C. 生成1mol氧化产物时转移电子数为4NA
D. 通常状况下11.2LCO2中含质子的数目为11NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将3.64 g Fe2O3和Al2O3的混合物溶于200 mL 0.1 mol/L盐酸中(盐酸过量),再向该溶液中加入NaOH溶液使Fe3+和Al3+恰好完全沉淀,用去NaOH溶液100 mL。则NaOH溶液的物质的量浓度是( )
A. 0.1 mol/L B. 0.2 mol/L C. 0.4 mol/L D. 0.8 mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨硼烷(NH3·BH3)电池可在常温下工作,装置如图所示。该电池工作时的总反应为:NH3·BH3+3H2O2=NH4BO2+4H2O。下列说法错误的是( )

A. 装置左侧电极为负极,电子由该极出发,依次通过正极、电解质溶液,回到负极
B. 正极的反应式为:H2O2+2H++2e-=2H2O
C. 电池工作时,H+通过质子交换膜向正极移动,
D. 消耗3.lg氨硼烷,理论上转移0.6mol电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上以钛铁矿(主要成分为钛酸亚铁( FeTiO3),含有MgO、SiO2等杂质)为原料,制备金属钛和铁红的工艺流程如下:

已知:①酸浸时, FeTiO3转化为Fe2+和TO2+;②本实验温度下,Ksp[Mg(OH)2]=1.0×10-11;③溶液中离子浓度小于等于1.0×10-5mol/L时,认为该离子沉淀完全。
请回答下列问题:
(1)酸浸时如何提高浸取速度和浸取率________(至少答两种方法)
(2)“水解”生成H2TiO3的离子方程式为________。
(3)“沉铁”过程中,气态产物的电子式为__________;该过程需控制反应温度低于35℃,原因为_______。
(4)滤液3可用于制备Mg(OH)2。若滤液3中c(Mg2+)=1.2×10-3mo/L,向其中加入NaOH固体,调整溶液pH值大于________时,可使Mg2+恰好沉淀完全。
(5)“电解”时,电解质为熔融的CaO,两电极材料为石墨棒。则_______极石墨棒需要定期更换,原因是________。
(6)测定铁红产品纯度:称取m克铁红,溶于一定量的硫酸之中,配成500.00mL溶液。从其中量取20.00mL溶液,加入过量的KI,充分反应后,用 c mol/L硫代硫酸钠(Na2S2O3)标准液滴定至终点,发生反应:I2+2S2O32-=S4O62-+2I-。平行滴定三次,硫代硫酸钠平均消耗体积为VmL。则铁红产品的纯度为:________(用c、V、m表式)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分析下图的能量变化示意图,下列选项正确的是( )

A. C(g)=A(g)+1/2B(g) △H>0 B. 2C=2A+B △H>0
C. 2A(g)+B(g)=2C(g) △H>O D. A(g)+1/2B(g)=C(g) △H<0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铂钻合金是以铂为基含钻二元合金,在高温下,铂与钻可无限互溶,其固溶体为面心立方晶格。铂钻合金磁性极强,磁稳定性较高,耐化学腐蚀性很好,主要用于航天航空仪表电子钟表磁控管等。
(1)基态钴原子的价电子排布图为______。
(2)二氯二吡啶合铂是由Pt2+、Cl-和吡啶结合形成的铂配合物,有顺式和反式两种同分异构体(如图)。科学研究表明,顺式分子具有抗癌活性。

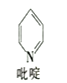
①吡啶分子是大体积平面配体,其结构简式如图所示,每个分子中含有的σ键数目为______。二氯二吡啶合铂分子中所含的C、N、Cl三种元素的第一电离能由大到小的顺序是______。
②二氯二吡啶合铂中存在的微粒间作用力有______(填字母)。
a.范德华力b.氢键c.金属键d非极性键
③反式二氯二吡啶合铂分子是______(填“极性分子”或“非极性分子”)。
(3)某研究小组将平面型的铂配合物分子进行层状堆砌,使每个分子中的铂原子在某一方向上排列成行,构成能导电的“分子金属”,其结构如图所示。

①“分子金属”可以导电,是因为______能沿着其中的金属原子链流动。
②“分子金属”中,铂原子是否以sp3的方式杂化?______(填“是”或“否”),其理由是______。
(4)筑波材料科学国家实验室一个科研小组发现了在5K下呈现超导性的晶体CoO2,该晶体具有层状结构(如图所示,小球表示Co原子,大球表示O原子),图中用粗线画出的重复结构单元示意图不能描述CoO2的化学组成的是______(填字母)。

(5)金属铂品体中,铂原子的配位数为12,其立方晶胞沿式x、y或z轴的投影图如图所示,若金属铂的密度为dgm-3,则晶胞参数a=______nm(列计算式)。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】人体血液存在H2CO3/HCO3—、HPO42-/H2PO4—等缓冲对。常温下,水溶液中各缓冲对的微粒浓度之比的对数值lg x[x表示![]() 或
或![]() ]与pH的关系如图所示。已知碳酸pKal═6.4、磷酸pKa2═7.2 (pKa═ -lgKa)。则下列说法不正确的是
]与pH的关系如图所示。已知碳酸pKal═6.4、磷酸pKa2═7.2 (pKa═ -lgKa)。则下列说法不正确的是

A. 曲线Ⅱ表示lg![]() 与pH的变化关系
与pH的变化关系
B. a~b的过程中,水的电离程度逐渐增大
C. 当c(H2CO3) ═c (HCO3—)时,c(HPO42—)=c(H2PO4—)
D. 当pH增大时,![]() 逐渐增大
逐渐增大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com