
分析 (1)H2SO3酸性小于盐酸,所以SO2和BaCl2溶液不反应;
(2)SO2和NaOH溶液反应生成Na2SO3,Na2SO3和BaCl2发生复分解反应;亚硫酸盐沉淀能溶于稀盐酸;
(3)氯气具有强氧化性,SO2具有还原性,二者在水溶液里发生氧化还原反应生成H2SO4和盐酸,硫酸和氯化钡发生复分解反应;
(4)B是硫酸钡,根据S原子守恒计算SO2的物质的量,再结合转移电子守恒计算氯气的体积.
解答 解:(1)H2SO3酸性小于盐酸,亚硫酸和BaCl2混合不符合复分解反应的条件,所以SO2和BaCl2溶液不反应,故答案为:不反应;H2SO3酸性小于盐酸;
(2)SO2和NaOH溶液反应生成亚硫酸钠,亚硫酸钠和BaCl2发生复分解反应生成BaSO3,所以A为BaSO3,BaSO3能溶于稀盐酸,故答案为:BaSO3;
(3)氯气具有强氧化性,二氧化硫具有还原性,二者在水溶液里发生氧化还原反应生成硫酸和盐酸,硫酸和氯化钡发生复分解反应,离子方程式为2H2O+SO2+Cl2+Ba2+=BaSO4↓+2Cl-+4H+,故答案为:2H2O+SO2+Cl2+Ba2+=BaSO4↓+2Cl-+4H+;
(4)B是硫酸钡,n(BaSO4)=$\frac{2.33g}{233g/mol}$=0.01mol,根据S原子守恒知n(BaSO4)=n(SO2)=0.01mol,
根据转移电子守恒知参加反应的n(SO2)=n(Cl2)=0.01mol,则V(Cl2)=0.01mol×22.4L/mol=0.224L=224mL,
故答案为:224.
点评 本题考查二氧化硫、氯气的性质,知道二氧化硫和氯气在水溶液中发生的反应是解本题关键,熟练运用原子守恒、转移电子守恒进行计算,题目难度不大.


 应用题作业本系列答案
应用题作业本系列答案科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该反应中氧化剂与氧化产物的物质的量之比为4:1 | |
| B. | 生成3.2g S同时放出4.48LNO2 | |
| C. | AgI的悬浊液中滴加Na2S溶液可转化成黑色沉淀 | |
| D. | 若将产物NO2收集于密闭容器里再置于热水中,气体颜色变浅 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 只有非金属原子间才能形成共价键 | |
| B. | 有化学键断裂的变化属于化学变化 | |
| C. | 由共价键形成的物质-定是共价化合物分子 | |
| D. | 离子化合物中可能含有共价键,而共价化合物中一定不含离子键 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 组别 | 草酸的体积(mL) | 温度 | 其他物质 |
| ① | 2Ml | 20 | 无 |
| ② | 2mL | 20 | 10滴饱和MnS04溶液 |
| ③ | 2mL | 30 | 无 |
| ④ | 1mL | 20 | 1mL蒸馈水 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
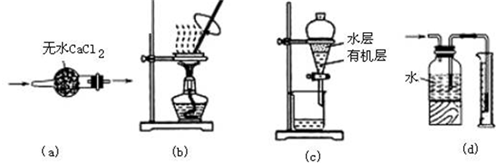
| A. | 用图a所示装置干燥NH3气体 | |
| B. | 用图b所示装置蒸发NaCl溶液得NaCl晶体 | |
| C. | 用图c所示装置分离有机层与水层,水层从分液漏斗下口放出 | |
| D. | 用图d所示装置测量氯气的体积 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验操作 | 现象 | 解释或结论 |
| A | 向某溶液中加入足量稀盐酸无现象,再滴加BaCl2溶液 | 有白色沉淀生成 | 原溶液中有SO42- |
| B | Agl沉淀中滴入稀KCl溶液 | 有白色沉淀生成 | AgCl比AgI更难溶 |
| C | 向CH3CH2X中加入少量AgNO3溶液,加热 | 有浅黄色沉淀生成 | CH3CH2X中含有Br- |
| D | C2H5OH与浓硫酸170℃共热,制得的气体通入酸性KMnO4溶液 | KMnO4溶液褪色 | 使KMnO4溶液褪色的是乙烯 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | (3a+0.5b)mol | B. | (3a+0.5b)mol | C. | (3a+0.5b+3p)mol | D. | (3a+0.5b-3p)mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②③ | B. | ③④ | C. | ①③ | D. | ①④ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com