
下列说法正确的是( )
A. 需要加热方能发生的反应一定是吸热反应 B.放热反应在常温下一定很容易发生
C.反应是放热还是吸热,必须看反应物和生成物所具有的总能量的相对大小
D.化学反应只生成新物质,没有能量的变化
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
在无色透明的酸性溶液中,能较大量共存的离子组是( )
A. MnO4-、K+、SO42-、Na+ B. Na+、SiO32-、K+、NO3-
C. NH4+、NO3-、Al3+、Cl- D. K+、SO42-、HCO3-、Na+
查看答案和解析>>
科目:高中化学 来源: 题型:
在2L的密闭容器中,充入1mol N2和 3mol H2,在一定条件下反应,2分钟后达到平衡状态,相同温度下,测得混合气体平衡时的压强比反应前混合气体的压强减小1/10,请问:
(1)平衡时混合气体中三种气体物质的量之比为n(N2):n(H2):n(NH3)= 。
(2)N2的转化率为 。
(3)2分钟内,NH3的平均反应速率为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
反应A+B===2C,在反应过程中,断裂1mol A中的化学键消耗的能量为Q1 kJ,断裂1mol B中的化学键消耗的能量为Q2 kJ,形成1mol C中的化学键释放的能量为Q3 kJ;1mol A所含化学能为E1 kJ, 1mol B所含化学能E2 kJ,1molC 所含化学能E3 kJ。下列说法中一定正确的是( )
A.若Q1+Q2 < Q3,则反应为放热反应 B.若Q1+Q2 > Q3,则反应为放热反应
C.若E 1+E 2 >E 3,则反应为放热反应 D.若E 1+E 2 >E 3,则反应为吸热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
下面是甲、乙、丙3位同学制取乙酸乙酯的过程,请你参与并协助他们完成相关的实验任务
【实验目的】制取乙酸乙酯
【实验原理】甲、乙、丙3位同学均采取乙醇、乙酸与浓硫酸混合共热的方法制取乙酸乙酯。
【装置设计】甲、乙、丙3位同学分别设计了下列3套实验装置:

若从甲、乙两位同学设计的装置中选择1套作为实验室制取乙酸乙酯的装置,应该选择的装置是____(填“甲”或“乙”)。丙同学将甲装置中的玻璃导管改成了球形干燥管,除起导气和冷凝作用外,另一个重要的作用是________________________。
【实验步骤】
a.按所选择的装置组装仪器,在试管①中先加入3mL95%的乙醇,并在摇动下缓缓加入2mL浓硫酸,充分摇匀,冷却后再加入2mL冰醋酸;
b.将试管固定在铁架台上;c.在试管②中加5mL饱和Na2CO3溶液;
d.用酒精灯对试管①加热;e.当观察到试管②中有明显现象停止实验。
【问题讨论】
(1)步骤a中组装好实验装置后,加入样品前还应________________________。
(2)试管②中装有饱和Na2CO3溶液,其作用是_______(填字母)。
A. 吸收乙醇 B. 中和乙酸
C. 乙酸乙酯在饱和Na2CO3溶液中的溶解度更小,有利于分层析出
D. 加速酯的生成,提高其产率
(3)根据试管②中观察到的现象,可知乙酸乙酯的物理性质有_ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下表中的污染与其来源不对应的是( )
| A | B | C | D | |
| 污染 | 白色污染 | PM | 氮氧化物 | 水体富营养化 |
| 来源 | 废弃塑料 | 化石燃料燃烧 | 汽车尾气 | 石油化工废弃物 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法不正确的是( )
A.汽车尾气中有NOx,主要是汽油不充分燃烧引起的
B.发泡塑料饭盒主要材质是高分子材料,不适于盛放含油较多的食品
C.BaSO4难溶于水,医疗上可用做钡餐
D.为改善食物的色、香、味并防止变质,可在其中加入适量食品添加剂
查看答案和解析>>
科目:高中化学 来源: 题型:
高铁酸钾(K2FeO4)是一种集氧化、吸附、絮凝于一体的新型多功能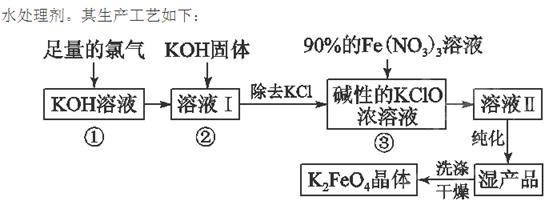 (1)反应①应在温度较低的情况下进行。因在温度较高时KOH与Cl2反应生成的是KClO3。写出在温度较高时KOH与Cl2反应的化学方程式 ,该反应的氧化产物是 。
(1)反应①应在温度较低的情况下进行。因在温度较高时KOH与Cl2反应生成的是KClO3。写出在温度较高时KOH与Cl2反应的化学方程式 ,该反应的氧化产物是 。
(2)在溶液Ⅰ中加入KOH固体的目的是 (填编号)。
A.与溶液Ⅰ中过量的Cl2继续反应,生成更多的KClO
B.KOH固体溶解时会放出较多的热量,有利于提高反应速率
C.为下一步反应提供碱性的环境
D.使KClO3转化为KClO
(3)从溶液Ⅱ中分离出K2FeO4后,还会有副产品KNO3、KCl,则反应③中发生的离子反应方程式为 。
(4)如何判断K2FeO4晶体已经洗涤干净 。
(5)高铁酸钾(K2FeO4)作为水处理剂的一个优点是能与水反应生成胶体吸附杂质,配平该反应的离子方程式:
___FeO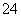 +____H2O — ____Fe(OH)3(胶体)+____O2↑+____OH-。
+____H2O — ____Fe(OH)3(胶体)+____O2↑+____OH-。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com