
【题目】固体硝酸盐加热易分解且产物较复杂,某学习小组以Fe(NO3)2为研究对象,通过实验探究其热分解的产物,查阅资料,根据硝酸盐受热分解的规律,提出如下4种猜想:
甲:Fe2O3、NO2乙:Fe2O3、NO2、O2丙:Fe3O4、NO2、O2丁:FeO、NO2、N2
(1).实验前,小组成员经讨论认定猜想丁不成立,理由是__________________.
针对上述猜想,设计如图所示的实验装置(图中加热、夹持仪器等均省略):
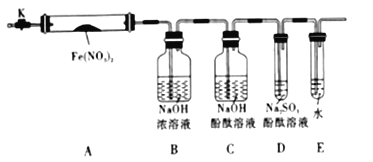
(2).实验过程
①仪器连接后,放人固体试剂之前,应______________
②称取Fe(NO3)2固体3.6g置于A中,加热前先打开K,___________,后再关闭K,用酒精灯加热
③观察到A中有红棕色气体出现,C、D中未见明显变化.
④待样品完全分解,A装置冷却至室温、称量,测得剩余固体的质量为1.6g
⑤取少量剩余固体于试管中,加人适量水,未见明显现象.
(3).实验结果分析讨论:
①根据实验现象和剩余固体的质量经分析,可初步确认分解产物中有____________。
②根据D中无明显现象,一位同学认为不能确认分解产物中有O2,因为若有O2,D中溶液颜色会退去;另一个同学认定分解产物中有O2存在,未检侧到的原因是_________________。
③为了验证是否有O2,某同学另称Fe(NO3)2固体3.6g,充分加热,收集气体,假设产生的气体全部收集,将集满气体的试管倒放在水槽中,观察到的现象是红棕色消失,液面上升,进入试管中的溶液大于2/3,通入一定量的O2后,气体全部被吸收,请写出Fe(NO3)2受热分解的化学方程式______________,通入O2的物质的量为_____________。
④小组讨论后达成的共识是上述实验设计仍不完善,需改进装置进一步研究。写一点不足之处:__________________________。
【答案】(1).不符合氧化还原反应原理(2分)
(2).①检验装置的气密性(1分)
②通入N2充满整个装置(2分)
(3)①Fe2O3、NO2(2分)②NO2和O2按4:1完全溶于溶液中(2分)
③4Fe(NO3)2![]() 2Fe2O3+8NO2↑+O2↑(2分) 0.005mol(2分)
2Fe2O3+8NO2↑+O2↑(2分) 0.005mol(2分)
④在A和B处加一个防倒吸的装置或者产生的气体不易收集(合理即给分)(2分)
【解析】
试题分析:(1)根据氧化还原反应原理有化合价的升高就有化合价的降低,而丁中只有化合价的降低,故不可能。
(2)该实验是通过定量和定性相结合的方法进行探究,通过固体质量的减少可以确定剩余的固体产物;通过红棕色气体,说明有NO2气体,排除丙的可能。①一个完整的实验流程:安装,检查气密性,装药,实验,拆装置……,该过程为检查气密性;②该实验过程中要排除氧气的干扰,故先用氮气排除空气,加热的操作时先预热,再对准一点加热。
(3)①红棕色气体是二氧化氮;硝酸亚铁的物质的量是0.02mol,全部转化为氧化铁是0.01mol,质量是1.6g,剩余的固体恰好是1.6g,则分解产物中有氧化铁和NO2;②由于NO2和O2按4:1完全溶于溶液中,所以没有检测到氧气;③将集满气体的试管倒放在水槽中,观察到的现象是红棕色消失,液面上升,进入试管中的溶液大于2/3,通入一定量的O2后,气体全部被吸收,这说明生成的NO2的体积大于4倍氧气的体积,因此Fe(NO3)2受热分解的化学方程式为4Fe(NO3)2![]() 2Fe2O3+8NO2↑+O2↑。生成NO2是0.04mol,完全溶解需要0.01mol氧气,而生成的氧气只有0.005,所以还需要再通入0.005mol氧气。
2Fe2O3+8NO2↑+O2↑。生成NO2是0.04mol,完全溶解需要0.01mol氧气,而生成的氧气只有0.005,所以还需要再通入0.005mol氧气。
④由于NO2溶于水容易产生倒吸现象,因此改进的措施是在A和B处加一个防倒吸的装置或者产生的气体不易收集。


科目:高中化学 来源: 题型:
【题目】在1L含0.2molKOH、0.1molNaAlO2和0.1 mol Ba(NO3) 2 的混合溶液中,逐滴加入浓度为0.1 mol/L 的H 2 SO 4 溶液,下列图像中能表示反应产生的沉淀的物质的量和所加入硫酸溶液的体积关系是(已知AlO2-和Ba2+可以大量共存)

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“神舟”飞船成功发射,标志着我国航天科技达到了较高水平。为了降低宇航员所在轨道舱和返回舱内二氧化碳的浓度,同时释放氧气,舱内放入下列哪种物质能满足上述要求
A.H2O B.Na2O2 C.KClO3 D.KMnO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于物质的量浓度表述正确的是
A.0.2mol·L-1 Na2SO4溶液中含有Na+和SO42—总物质的量为0.6mol
B.50mL 2mol·L-1的NaCl溶液和100 mL L 0.5mol·L-1MgCl2溶液中,Cl-的物质的量浓度相等
C.用1L水吸收22.4L氯化氢(标况下)所得盐酸的浓度是1mol·L-1
D.10g 98%的硫酸(密度为1.84g·cm—3)与10mL 18.4mol·L—1的硫酸的浓度是相同的
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二水合重重铬酸钠(Na2Cr2O7.2H2O),[已知M(Na2Cr2O7.2H2O)=298g/mol]俗称红矾钠,在工业方面有广泛用途。我国目前主要是以铬铁矿(主要成份为FeO.Cr2O3,还含有A1203、MgO、Si02等杂质)为主要原料生产,其主要工艺流程如图:
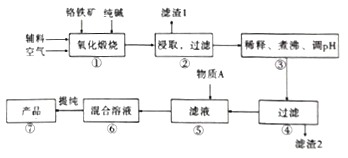
已知信息:
Ⅰ.“①”中涉及的主要反应是:4FeO·Cr2O3+8Na2CO3+7O2=8Na2CrO4+2Fe2O3+8CO2
Ⅱ.部分阳离子以氢氧化物形式完全沉淀时溶液的PH如下:
沉淀物 | Al(OH)3 | Fe(OH)3 | Mg(OH)2 | Cr(OH)3 |
完全沉淀时溶液PH | 4.7 | 3.7 | 11.2 | 5.6 |
(1).杂质A12O3、SiO2与纯碱反应转变为可溶性盐,写出A12O3纯碱反应的化学方程式为:______________,滤渣1的主要成分为__________________。
(2).“③”中通过调节PH除去杂质,调节PH至___________。
(3).“⑤”中向滤液中加入物质A,得到Na2Cr2O3和Na2SO4的混合溶液,物质A为__________,简述原因:______________________________。(用离子方程式及文字加以说明)
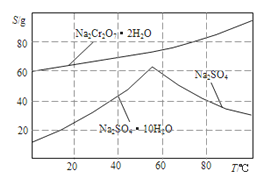
(4).如图是Na2Cr2O3.2H2O和Na2SO4的溶解度曲线。提纯的实验操作:将Na2Cr2O3和Na2SO4的混合溶液______________________,得到Na2SO4固体和较纯净的Na2Cr2O3溶液。
(5).实验室测定所得产品中红矾钠的纯度,称取产品3.2g,配成250mol溶液,取出25.00mL于锥形瓶中,加入10mL2mol/LH2SO4和足量碘化钾,放于暗处5min,写出离子方程式:________________。然后加水100mL,加入3mL淀粉指示剂,用0.1000mol/LNa2S2O3标准溶液滴定I2+2S2O32-=2I-+S4O62-若达到滴定终点时,共用去Na2S2O3标准溶液60mL,所得产品的纯度是_________(结果保留小数点后1位)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应的离子方程式不能用H++OH-=H2O表示的是( )
A. 硫酸氢钠和氢氧化钡 B. 氢氧化钾和盐酸
C. 硝酸和氢氧化钠 D. 氢氧化钡和硝酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高铁电池是电动汽车首选的电池之一,该电池的工作原理为:
3Zn+2K2FeO4+8H2O![]() 3Zn(OH)2+2Fe(OH)3+4KOH,
3Zn(OH)2+2Fe(OH)3+4KOH,
下列关于该电池放电时的说法中正确的是( )
A.高铁电池产生的电流从负极经外电路到达正极
B.正极反应式为Zn+2OH--2e - =Zn(OH)2
C.负极pH减小,正极pH增大,电解液pH增大
D.每氧化1mol高铁酸钾转移3mol电子
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com