
| A、反应后溶液中不存在任何沉淀,所以反应前后Cu2的浓度不变 |
| B、沉淀溶解后,深蓝色的溶液为[Cu(NH3)4](OH)2 |
| C、在[Cu(NH3)4]2+离子中,Cu2+给出孤对电子NH3提供空轨道 |
| D、用硝酸铜溶液代替硫酸铜溶液进行实验,能观察到同样的现象 |


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
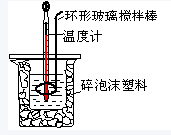
| 起始温度/℃ | 终止温度/℃ | 温度差/℃ | |||
| HCl | NaOH | 平均值 | |||
| 1 | 25.5 | 25.0 | 25.25 | 28.5 | 3.25 |
| 2 | 24.5 | 24.2 | 24.35 | 27.6 | 3.25 |
| 3 | 25.0 | 24.5 | 24.75 | 26.5 | 1.75 |
查看答案和解析>>
科目:高中化学 来源: 题型:
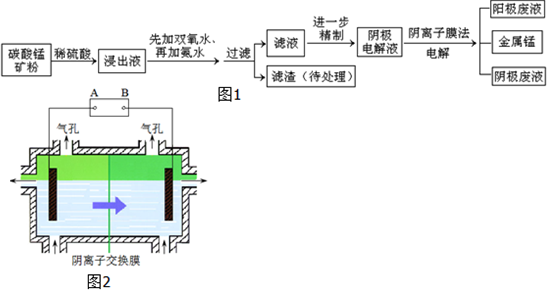
| 离子 | Fe3+ | Al3+ | Fe2+ | Mn2+ | Mg2+ |
| 开始沉淀的pH | 2.7 | 3.7 | 7.0 | 7.8 | 9.3 |
| 沉淀完全的pH | 3.7 | 4.7 | 9.6 | 9.8 | 10.8 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
A、由2Cu+O2
| ||||
| B、Fe3O4可表示为FeO?Fe2O3,则Pb3O4可表示为PbO?Pb2O3 | ||||
| C、过量的CO2与石灰水反应生成Ca(HCO3)2,过量CO2通入漂白粉溶液中,产物是Ca(HCO3)2和HClO | ||||
| D、CO2与过氧化钠反应只生成Na2CO3和O2故SO2与过氧化钠一定生成Na2SO3和O2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
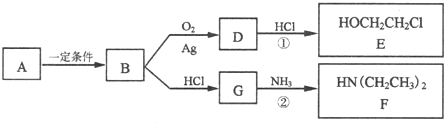
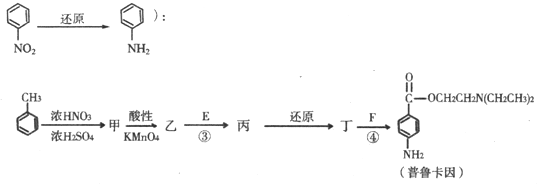
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com