
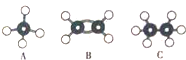
 现有A、B、C三种烃,其球棍模型如图:
现有A、B、C三种烃,其球棍模型如图: .
.分析 由A、B、C三种烃的球棍模型图可知,A为甲烷,B为乙烯,C为乙烷,
(1)生成水物质的量是二氧化碳物质的量的两倍,由n(H2O)=2n(CO2),则C、H原子个数比为1:2;
(2)碳原子介于4到10的该系列物质,核磁共振氢谱只有一种峰的物质,结构中只有1种H;
(3)碳正离子CH5+可以通过CH4在“超强酸”中再获得一个H+而得到,而CH5+失去H2可得CH3+;
(4)(CH3)3C+失去一个H+后将生成乙烯的同系物F,F为CH2=C(CH3)2.
解答 解:(1)生成水物质的量是二氧化碳物质的量的两倍,由n(H2O)=2n(CO2),则C、H原子个数比为1:4,只有CH4符合,故答案为:CH4;
(2)碳原子介于4到10的该系列物质,核磁共振氢谱只有一种峰的物质,结构中只有1种H,结构简式分别是C(CH3)4、(CH3)3CC(CH3)3,故答案为:AC;C(CH3)4;CH3)3CC(CH3)3;
(3)碳正离子CH5+可以通过CH4在“超强酸”中再获得一个H+而得到,而CH5+失去H2可得CH3+,CH3+中4个原子是共平面的,三个键角相等,键角应是120°;电子式为 ,故答案为:120°;
,故答案为:120°; ;
;
(4)(CH3)3C+失去一个H+后将生成B的同系物F,F为CH2=C(CH3)2,故答案为:CH2=C(CH3)2.
点评 本题考查有机物的结构与性质,为高频考点,把握官能团及性质、结构的对称性为解答的关键,侧重分析能力及结构中H种类的判断的考查,题目难度不大.


 优生乐园系列答案
优生乐园系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 950mL,111.2g | B. | 1000 mL,117.0g | C. | 500mL,117g | D. | 任意规格,111.2g |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 如图所示装置中,甲、乙、丙三个烧杯依次分别盛放足量的NaOH溶液、足量的CuSO4溶液、足量的Na2SO4溶液,电极均为石墨电极.接通电源,经过一段时间后,测得乙中c电极质量增加.据此回答下列问题:
如图所示装置中,甲、乙、丙三个烧杯依次分别盛放足量的NaOH溶液、足量的CuSO4溶液、足量的Na2SO4溶液,电极均为石墨电极.接通电源,经过一段时间后,测得乙中c电极质量增加.据此回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用铜作电极电解NaCl溶液:2Cl-+2H2O$\frac{\underline{\;通电\;}}{\;}$Cl2↑+H2↑+2OH- | |
| B. | 常温下,向醋酸钠溶液中滴加少量醋酸使溶液的pH=7,则混合溶液中:c(Na+)=c(CH3COO-) | |
| C. | 磷酸一氢钠溶液水解:HPO42-+H2O?PO42-+H3O+ | |
| D. | 常温下,由水电离产生的c(H+)=10-12mol•L-1的溶液,NH4+、SO42-、HCO3-、Cl-能大量共存 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 钾的原子质量就是钾的相对原子质量 | |
| B. | 一个硫原子的实际质量约等于$\frac{32}{(6.02×1{0}^{23})}$g | |
| C. | 水的相对分子质量为18g | |
| D. | 17g OH-中所含电子数为9NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
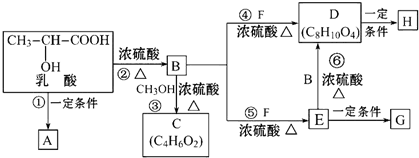
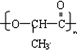 ;
; .
.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 按要求完成硝酸钾晶体的制备实验:
按要求完成硝酸钾晶体的制备实验:| 步骤 | 操作 | 具体操作步骤 | 现象解释结论等 |
① | 溶解 | 取20克KNO3和17克NaCl溶解在35ml水中,加热至沸,并不断搅拌. | 固体溶解 |
| ② | 蒸发 | 继续加热搅拌,使溶液蒸发浓缩. | 有a晶体析出. |
| ③ | 热过滤 | 当溶液体积减少到约原来的一半时,迅速趁热过滤 | 滤液中的最主要成分为b. |
| ④ | 冷却 | 将滤液冷却至室温. | 有晶体析出. |
| ⑤ | 按有关要求进行操作 | 得到初产品硝酸钾晶体 | |
⑥ | 将得到的初产品硝酸钾晶体溶于适量的水中,加热、搅拌,待全部溶解后停止加热,使溶液冷却至室温后抽滤. | 得到纯度较高的硝酸钾晶体 | |
| ⑦ | 检验 | 分别取⑤、⑥得到的产品,配置成溶液后分别加入1滴1mol/l的HNO3和2滴0.1mol/l的AgNO3 | 可观察到⑤、⑥产品中出现的现象分别是⑤产品中产生白色沉淀,⑥产品中无明显现象. |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com