
| A. | W与氢形成的原子比为1:1的化合物有多种 | |
| B. | X的氢化物只含有极性共价键 | |
| C. | Y单质可通过电解Y的氯化物获得 | |
| D. | W与Z形成化合物WZ2中各原子均满足8电子稳定结构 |
分析 W的一种核素在考古时常用来鉴定一些文物的年代,用的是C14,则W为C元素;X2-和Y2+具有相同的电子层结构,X为O、Y为Mg,Z原子的最外层电子数是其电子层数的2倍,应为S元素,结合元素周期律的递变规律解答该题.
解答 解:由以上分析可知W为C、X为O、Y为Mg、Z为S元素.
A.C与H元素的形成的苯、乙炔等化合物的C、H原子比为1:1,故A正确;
B.X为O,与H形成的过氧化氢中既含有极性键也含有非极性键,故B错误;
C.工业用电解熔融的氯化镁的方法冶炼镁,故C正确;
D.CS2中存在C=S键,各原子均满足8电子稳定结构,故D正确.
故选B.
点评 本题考查原子结构与元素周期律的关系,为高考常见题型,侧重考查学生的分析能力,题目难度中等,本题注意正确推断元素的种类为解答该题的关键,易错点为A,注意碳氢化合物的种类以及性质.


科目:高中化学 来源: 题型:选择题
| A. | 向偏铝酸钠溶液中滴加碳酸氢钠溶液:AlO2-+HCO3-+H2O═Al(OH)3↓+CO32- | |
| B. | Fe(NO3)3溶液中通入足量SO2:2Fe3++SO2+2H2O═2Fe2++SO42-+4H+ | |
| C. | 酸性KMnO4溶液与H2O2反应证明H2O2具有还原性:MnO4-+10H++H2O2═2Mn2++6H2O | |
| D. | 澄清的石灰水中加入过量的NaHCO3溶液:Ca2++OH-+HCO3-═CaCO3↓+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在周期表中处于第3周期 VIIA | B. | 在周期表中处于第2周期VA族 | ||
| C. | 氢化物比PH3稳定 | D. | 常见化合价有-3、+2、+3、+5价 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
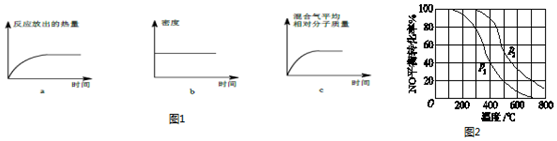
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 ,关于有机物A的说法不正确的是( )
,关于有机物A的说法不正确的是( )| A. | A的分子式为C16H14O3 | |
| B. | A可使酸性KMnO4溶液和溴水褪色 | |
| C. | A苯环上的一氯代物同分异构体有2种 | |
| D. | A既可发生氧化反应和加成反应,也可以发生取代反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
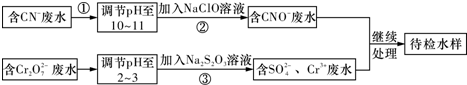
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
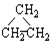 ③CH3CH2CH3 ④HC≡C-CH3.
③CH3CH2CH3 ④HC≡C-CH3.| A. | ①和② | B. | ①和③ | C. | ①和④ | D. | ②和④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.6 | B. | 0.7 | C. | 0.75 | D. | 0.8 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com