
【题目】Na2S2O3是重要的化工原料,用途很广,其还原性较强,在溶液中易被Cl2氧化成![]() ,常用作脱氯剂,主要用于治疗氰化物中毒。工业上可利用反应Na2CO3+2Na2S+4SO2===3Na2S2O3+CO2制取Na2S2O3,下列说法正确的是( )
,常用作脱氯剂,主要用于治疗氰化物中毒。工业上可利用反应Na2CO3+2Na2S+4SO2===3Na2S2O3+CO2制取Na2S2O3,下列说法正确的是( )
A. Na2S2O3只有还原性
B. 氧化产物与还原产物的物质的量之比为2∶1
C. 每生成1 mol Na2S2O3,转移4×6.02×1023个电子
D. 标准状况下,每吸收4 mol SO2就会放出22.4 L CO2
【答案】D
【解析】分析:根据硫化钠中硫元素化合价升高,二氧化硫中硫元素化合价降低,结合氧化还原反应的有关概念和电子得失守恒判断与计算。
详解:A. Na2S2O3中硫元素化合价是+2价,处于中间价态,既有还原性,也有氧化性,A错误;
B. 硫化钠中硫元素从-2价升高到+2价,失去电子被氧化。二氧化硫中硫元素化合价从+4价降低到+2价,得到电子被还原,因此氧化产物与还原产物的物质的量之比为1∶2,B错误;
C. 每生成3 mol Na2S2O3,转移8mol电子,则每生成1 mol Na2S2O3,转移8/3×6.02×1023个电子,C错误;
D. 根据方程式可知,每吸收4 mol SO2就会放出1mol二氧化碳,标准状况下体积为22.4 L,D正确,答案选D。


 寒假天地重庆出版社系列答案
寒假天地重庆出版社系列答案科目:高中化学 来源: 题型:
【题目】在a、b、c、d四个集气瓶中分别盛有H2、Cl2、HCl、HBr中的任一种气体,若将a和d两瓶气体混合后见光爆炸;若将a和b两瓶气体混合后,瓶壁上出现暗红色液滴,则a、b、c、d四个集气瓶中分别盛放的气体是( )
A.Cl2、H2、HCl、HBr B.Cl2、HCl、HBr、H2
C.Cl2、HBr、H2、HCl D.Cl2、HBr、HCl、H2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】胡椒酚是植物挥发油中的一种成分。关于胡椒酚的下列说法:

①该化合物属于芳香烃;
②分子中至少有7个碳原子处于同一平面;
③它的部分同分异构体能发生银镜反应;
④1 mol该化合物最多可与2 mol Br2发生反应。
其中正确的是( )
A. ②③ B. ①②④ C. ①③ D. ②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向mg镁和铝的混合物中加入适量的稀硫酸,恰好完全反应生成标准状况下的气体bL。向反应后的溶液中加入cmol/L氢氧化钾溶液VmL,使金属离子刚好沉淀完全,得到的沉淀质量为ng。再将得到的沉淀灼烧至质量不再改变为止,得到固体pg。则下列关系不正确的是( )
A. n=17Vc+m B. 5m/3<p<17m/9
C. p=m+cV/125 D. c=1000b/11.2V
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上以铬铁矿(主要成分为FeO·Cr2O3)、碳酸钠、氧气和硫酸为原料生产重铬酸钠(Na2Cr2O7),其主要反应为
①4FeO·Cr2O3+8Na2CO3+7O2![]() 8Na2CrO4+2Fe2O3+8CO2
8Na2CrO4+2Fe2O3+8CO2
②2Na2CrO4+H2SO4![]() Na2SO4+Na2Cr2O7+H2O
Na2SO4+Na2Cr2O7+H2O
下列说法中正确的是( )
A. 反应①和②均为氧化还原反应
B. 反应①,转移4 mol电子时,被氧化的为O2为1mol
C. 反应①的氧化剂是O2,还原剂是FeO·Cr2O3
D. 生成1 mol Na2Cr2O7时共转移5 mol电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列各组离子在指定溶液中一定能大量共存的是( )
A. 0.1 mol·L-1NaOH溶液:K+、Na+、SO42-、CO32-
B. 0.1 mol·L-1Na2CO3溶液:K+、Ba2+、NO3-、Cl-
C. 0.1 mol·L-1FeCl3溶液:K+、NH4+、I-、SCN-
D.  =1×1014的溶液:Ca2+、Na+、ClO-、NO3-
=1×1014的溶液:Ca2+、Na+、ClO-、NO3-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.氢化钙是固体登山运动员常用的能源提供剂.某兴趣小组拟选用如下装置制备氢化钙.
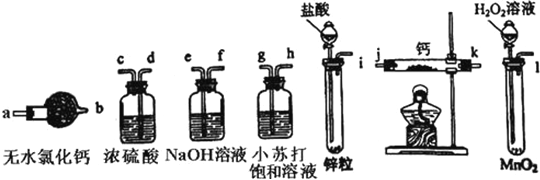
请回答下列问题:
(1)请选择必要的装置,按气流方向连接顺序为__________(填仪器接口的字母编号)
(2)根据完整的实验装置进行实验,实验步骤如下:检查装置气密性后,装入药品;打开分液漏斗活塞_________(请按正确的顺序填入下列步骤的标号).
A.加热反应一段时间 B.收集气体并检验其纯度
C.关闭分液漏斗活塞 D.停止加热,充分冷却
(3)已知钙与氢化钙固体在外观上相似,现设计一个实验,用化学方法区分钙与氢化钙,请完善以下实验的简要步骤及观察到的现象:取适量氢化钙,在加热条件下与________反应,将反应气相产物通过装有_______的容器,观察到容器内固体颜色变化为________;取钙做类似实验,观察不到类似的反应现象.
II.某化学兴趣小组发现,往CuSO4溶液中加入一定浓度的Na2CO3溶液得到的蓝色沉淀,若加入NaOH溶液则得到浅绿色沉淀。为此,小组同学对蓝色沉淀成份作了如下探究:
该小组同学利用下列装置通过实验测定其组成
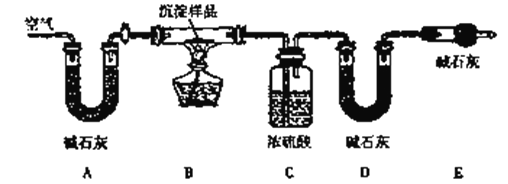
(1)检查装置气密性并装好药品后,点燃酒精灯前应进行的操作是______________。
(2)通过查找资料得知,该浅绿色沉淀物可能是溶解度最小的碱式硫酸铜(化学式CuSO4·3Cu(OH)2)。请你设计一个实验,证明浊液中的浅绿色沉淀物中是否含有硫酸根离子的方法__________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物X是一种香料,可采用乙烯与甲苯为主要原料,按下列路线合成:
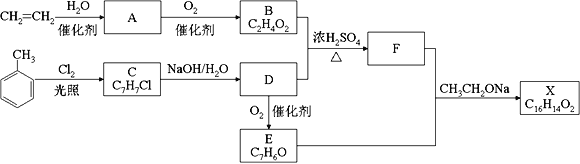
已知:RX![]() ROH;RCHO+CH3COOR’
ROH;RCHO+CH3COOR’![]() RCH=CHCOOR’
RCH=CHCOOR’
请回答:
(1) A中官能团的名称是______________________。
(2) D→E的化学方程式________________________________________________。
(3) X的结构简式_________________。
(4)与F互为同分异构体又满足下列条件的有_______种。
①遇到氯化铁溶液会显紫色,②会发生银镜反应 ③苯环上有三个取代基
在其它同分异构体中核磁共振氢谱有六组峰,氢原子数比符合1:2:2:2:2:1的结构为_____。
(5)根据上面合成信息及试剂,写出以乙烯为原料(无机试剂任选),写出合成CH3CH=CHCOOCH2CH3路线_____________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com