
【题目】图中a、b、c、d、e、f表示元素周期表中部分短周期元素,下列叙述正确的是( )

A.a、b、c的简单离子中,b的离子半径最大
B.c、d、f最高价氧化物对应的水化物两两之间均可发生反应
C.e的氢化物比f的氢化物的稳定性高
D.b、e可形成一种半导体材料
【答案】B
【解析】
a、b、c、d、e、f是短周期元素,由各元素在元素周期表中位置可知,a为氮元素、b为氧元素、c钠元素、d为铝元素、e为硅元素、f为氯元素。结合元素周期律和物质性质分析解答。
A、a为氮元素、b为氧元素、c钠元素,形成的离子电子层结构相同,电子层结构相同,核电荷数越大离子半径越小,所以a、b、c的简单离子中,c的离子半径最小,a的离子半径最大,A错误;
B、c为钠元素、d为铝元素、f为氯元素,最高价氧化物对应的水化物为氢氧化钠、氢氧化铝、高氯酸,氢氧化铝是两性氢氧化物,溶于氢氧化钠、高氯酸溶液,氢氧化钠与高氯酸发生中和反应,B正确;
C、e为硅元素、f为氯元素,非金属性Si<Cl,非金属性越强,氢化物越稳定,所以f的氢化物的稳定性高,C错误;
D.b、e形成的化合物是二氧化硅,不是半导体材料,可用于光导纤维,D错误。
答案选B。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】关于有机物a( )、b(
)、b(![]() -CH3)、c(
-CH3)、c(![]() )的说法正确的是
)的说法正确的是
A. a、b互为同分异构体 B. b、c均属于芳香化合物
C. c分子中所有碳原子共平面 D. a、b、c均能与溴水反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图A、B、C表示生物大分子,请分析推断并回答有关问题:

(1)请依次写出上图中X、Y所代表的元素:X为_______,Y为____。
(2)图中大分子物质A的中文名称是__________,其合成所需原料是_____________。
(3)B具有多样性,若从b分析其原因是_______________________________。若b的平均相对分子质量为110,通过②反应过程形成2条肽链,经盘曲折叠构成相对分子质量为3900的B,则B分子中肽键的数目是____。
(4)同一个人的肝细胞与骨骼肌细胞相比,A、B是否相同?________。
(5)导致地球上生物多种多样的根本原因是[]____的结构具有多样性。
(6)医学上进行器官移植时,和免疫排斥反应直接有关的结构是图中的___________。
(7)使用下列哪种物质处理会使细胞失去识别能力 (______)
A.核酸酶B.糖水解酶C.龙胆紫D.双缩脲试剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一体积不变的密闭容器中发生化学反应:2A(g) ![]() B(g)+C(g)。当物质A的起始浓度为1.0 mol·L-1、物质B、C的起始浓度为0时,物质A的浓度、转化率以及物质B的浓度随反应时间的变化如下列各图所示:
B(g)+C(g)。当物质A的起始浓度为1.0 mol·L-1、物质B、C的起始浓度为0时,物质A的浓度、转化率以及物质B的浓度随反应时间的变化如下列各图所示:

则下列有关说法中正确的是
A. 条件I、条件II时的反应温度不同,压强相同
B. 条件I时可能未使用催化剂,条件II时可能使用了催化剂
C. 条件III时的平衡混合物中,物质C的浓度等于0.6 mol·L-1
D. 条件IV和条件II相比较,条件IV时可能缩小了容器体积
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种有效治疗关节炎、脊椎炎等一些疾病的常用药物-菲诺洛芬钙,它的一种合成路线如下(具体反应条件和部分试剂略)

已知:①SOCl2可与醇发生反应,醇的羟基被氯原子取代而生成氯化烃
②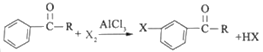 (X表示卤素原子)
(X表示卤素原子)
③R-X+NaCN![]() RCN+NaX
RCN+NaX
回答下列问题:
(1)B→C的反应类型是___________;写出D的结构简式:___________。
(2)F中所含的官能团名称是______________________。
(3)写出F和C在浓硫酸条件下反应的化学方程式______________________。
(4)A的同分异构体中符合以下条件的有___________种(不考虑立体异构)
①属于苯的二取代物; ②与FeCl3溶液发生显色反应。
其中核磁共振氢谱图中共有4个吸收峰的分子的结构简式为___________。
(5)结合上述推断及所学知识,参照上述合成路线任选无机试剂设计合理的方案,以苯甲醇(![]() )为原料合成苯乙酸苯甲酯(
)为原料合成苯乙酸苯甲酯(![]() )写出合成路线______________________,并注明反应条件。
)写出合成路线______________________,并注明反应条件。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关浓硫酸、浓盐酸、浓硝酸的认识不正确的是
A.浓硫酸、浓硝酸与金属反应时,分别是S、N得电子
B.蔗糖与浓硫酸混合后,白色蔗糖固体逐渐变成黑色疏松的碳,体现了浓硫酸的脱水性
C.浓盐酸、浓硝酸具有挥发性,而浓硫酸难挥发
D.常温下,浓硫酸或浓HNO3中投入Fe片,均会产生大量的气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液可能含有Cl-、SO42-、CO32-、NH4+、Fe3+、Fe2+、Al3+和Na+。某同学为了确认其成分,设计并完成了如下实验。由此可知原溶液中

A. 原溶液中c(Fe3+)=0.1 mol·L-1
B. 要确定原溶液中是否含有Fe2+,其操作如下:取少量原溶液于试管中,加KSCN溶液,再加入适量氯水,溶液呈血红色,则含有Fe2+
C. SO42-、NH4+、Na+一定存在,CO32-、Al3+一定不存在
D. 溶液中至少有4种离子存在,其中Cl-一定存在,且c(Cl-)≥0.2 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学习小组根据高中知识设计如下测定室内甲醛含量的装置(夹持及尾气处理等装置已略)。

Ⅰ.配制银氨溶液
(1)关闭K2和K3,打开K1和分液漏斗活塞,将饱和食盐水滴入到圆底烧瓶中,当观察到三颈烧瓶中最初生成的白色沉淀恰好完全溶解时,关闭K1和分液漏斗活塞。请写出三颈烧瓶中生成银氨溶液的化学方程式________________________。
II.测定室内空气中甲醛含量
(2)装置中毛细管的作用是________________________________________________。
(3)用热水浴加热三颈烧瓶,打开K3,将滑动隔板由最左端抽到最右端,吸入1L室内空气,关闭K3,后续操作是_________________________________________。共计进行上述操作十次。
(4)待甲醛充分被银氨溶液氧化为碳酸盐后,测得三颈瓶中共生成Ag 2.16mg。则空气中甲醛的含量为___________mg·L-1(空气中其它物质不与银氨溶液反应)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化学反应的热现象说法不正确的是( )
①放热反应发生时不必加热 ②化学反应一定有能量变化
③吸热反应需要加热后才能发生
④化学反应吸收或放出热量的多少与参加反应的物质多少有关
A.①②B.②③C.①③D.②④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com