
【题目】某待测溶液中可能含有SO42﹣、SO32﹣、CO32﹣、HCO3﹣、NO3﹣、Cl﹣、Br﹣中的若干种及一种常见金属阳离子(Mn+),现进行如下实验(每次实验所用试剂均是足量的,鉴定中某些成分可能没有给出).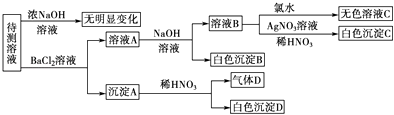
请回答下列问题:
(1)根据上述框图信息填写下表(不能确定的不填):
肯定存在的离子 | 肯定没有的离子 | |
化学式或离子符号 |
(2)出沉淀A三种可能的情况: , 若气体D遇空气变红棕色,则生成沉淀D时肯定发生的反应的离子方程式为 .
(3)若Mn+位于第三周期,则要确定它具体是何种离子的方法是 .
【答案】
(1)HCO3 ? ;Br﹣
(2)BaSO3;BaSO3、BaSO4;BaCO3、BaSO4;BaCO3、BaSO3;BaSO3、BaCO3、BaSO4;3BaSO3+2H++2NO3﹣═2NO↑+3BaSO4↓+H2O
(3)做焰色反应实验,观察到黄色火焰,则说明是钠
【解析】解:(1)沉淀A与稀硝酸反应仍得到白色沉淀知白色沉淀D为BaSO4 , 由于还生成气体D,气体D可能是稀硝酸与SO32﹣发生氧化还原反应生成的N0,还可能是稀硝酸与CO32﹣反应CO2 , 或两者均有,故溶液中SO42﹣、SO32﹣至少有一种,SO32﹣、CO32﹣至少有一种;由每次实验所用试剂均足量知溶液A中含有Ba2+ , 在加入碱后能得到白色沉淀B,则原待测溶液中一定含有HCO3﹣;溶液B中加入足量的氯水后仍得到无色溶液,说明原待测液中无Br﹣ , 不能确定是否有NO3﹣、CO32﹣、Cl﹣ , 根据以上分析可知,原待测溶液中一定含有HCO3﹣;一定没有无Br﹣;所以答案是:
肯定存在的离子 | 肯定不存在的离子 | |
化学式或离子符号 | HCO | Br﹣ |
·(2)沉淀A与稀硝酸反应仍得到白色沉淀知白色沉淀D为BaSO4 , 由于还生成气体D,气体D可能是稀硝酸与SO32﹣发生氧化还原反应生成的N0,还可能是稀硝酸与CO32﹣反应CO2 , 或两者均有,故溶液中SO42﹣、SO32﹣至少有一种,SO32﹣、CO32﹣至少有一种,故沉淀A可能只有BaSO3 , 可能为BaSO3、BaSO4 , 可能为BaCO3、BaSO4 , 可能为BaCO3、BaSO3 , 还可能为BaSO3、BaCO3、BaSO4;若气体D遇空气变红色时,表明D中肯定有NO,沉淀A中肯定有BaSO3 , 生成沉淀D的离子方程式为:3BaSO3+2H++2NO3﹣═2NO↑+3BaSO4↓+H2O,所以答案是:BaSO3;BaSO3、BaSO4;BaCO3、BaSO4;BaCO3、BaSO3;BaSO3、BaCO3、BaSO4;3BaSO3+2H++2NO3﹣═2NO↑+3BaSO4↓+H2O;(3)处于第三周期的金属阳离子有Na+、Mg2+、Al3+ , 由于Al3+与HCO3﹣不能大量共存,故金属阳离子不可能是Al3+ , 即Mn+只能是Na+或K+ , 可通过焰色实验来确定是镁还是钠,所以答案是:做焰色反应实验,观察到黄色火焰,则说明是钠.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】设NA表示阿伏加德罗常数的值,下列说法正确的是
A. 80℃时,1L pH=l的硫酸溶液中,含有的OH-数目为10-13NA
B. 向含有FeI2的溶液中通人适量氯气,当有1molFe2+被氧化时,该反应转移电子数目为3NA
C. l00g质量分数为46%的乙醇水溶液中氧原子数为4NA
D. 以Mg、Al为电极,NaOH溶液为电解质溶液的原电池中,导线上流过NA个电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组为探究铜跟浓硫酸的反应,用如下图所示装置进行有关实验。

(1)装置A中发生反应的化学方程式为_____________________________________
(2)装置D中试管口放置的棉花应浸一种溶液,这种溶液是________,其作用是____________________________________________________________________。
(3)装置B的作用是贮存多余的气体。当D处有明显的现象后,关闭旋塞K,移去酒精灯,但由于余热的作用,A处仍有气体产生,此时B中现象是_______________________,B中应放置的溶液是________。
a.水 b.酸性KMnO4溶液
c.浓溴水 d.饱和NaHSO3溶液
(4)实验中,取一定质量的铜片和一定体积18 mol·L-1的浓硫酸放在圆底烧瓶中共热,反应完毕时,发现烧瓶中还有铜片剩余,该小组学生根据所学的化学知识认为还有一定量的硫酸剩余,其原因是____________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以葡萄糖为燃料的微生物燃料电池结构示意图如图所示.关于该电池的叙述不正确的是( )
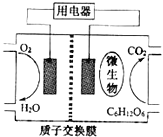
A.该电池能够在高温下工作
B.电池的负极反应为:C6H12O6+6H2O-24e-=6CO2+24H+
C.放电过程中,质子(H+)从负极区向正极区迁移
D.在电池反应中,每消耗1mol氧气,理论上能生成标准状况下CO2气体22.4 L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某lL混合溶液中所含离子的个数比如下表,则M离子可能为( )
所含离子 | NO3- | SO42- | H+ | M |
个数比 | 2 | 1 | 2 | 1 |
A.Mg2+B.Ba2+C.F-D.Na+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表为元素周期表的一部分。
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA |
1 | ① | ||||||
2 | ② | ⑤ | |||||
3 | ③ | ⑥ | |||||
4 | ④ | ⑦ | |||||
(1)表中元素________(填写元素符号)的非金属性最强;元素________(填写元素符号)的金属性最强,写出它与水反应的离子方程式__________________________________。
(2)表中元素③的原子结构示意图是________。
(3)表中元素⑥、⑦氢化物的稳定性顺序为________>________(填写化学式,下同)。
(4)表中元素最高价氧化物对应水化物酸性最强的酸的分子式是_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铟产业被称为“信息时代的朝阳产业”.元素周期表中铟的数据如图,下列说法完全正确的是( )

A. 铟元素的质量数是114.8
B. 铟元素的相对原子质量是114
C. 铟元素是一种副族元素
D. 铟原子核外有49个电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】天然气根据成分不同分为贫气和富气,贫气中甲烷的含量较多,富气中乙烷、丙烷、丁烷的含量相对高一些.若要将它们液化,下列说法正确的是( )
A.贫气易液化
B.富气易液化
C.二者液化条件相同
D.加压降温均有利于两者液化
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com