
| A. | 1.12 | B. | 2.24 | C. | 2.8 | D. | 4.48 |
分析 用极端法,假设0.15mol全是Fe时,发生反应Fe+H2SO4=FeSO4+H2
0.15mol 0.15mol
如果0.15mol全是Cu时,发生反应3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O
0.15mol 0.1mol
由此分析来确定X+Y的数值的范围.
解答 解:用极端法,假设0.15mol全是Fe时,发生反应Fe+H2SO4 =FeSO4+H2
0.15mol 0.15mol
如果0.15mol全是Cu时,发生反应3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O
0.15mol 0.1mol
所以X+Y的数值的范围在0.1mol×22.4L/mol=2.24~~~0.15mol×22.4L/mol=3.36之间
故选:C.
点评 本题考查金属混合物与酸反应来确定气体的体积,学生要学会用极端假设法来分析求解,首先确定范围,然后根据条件筛选,有一定的难度.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
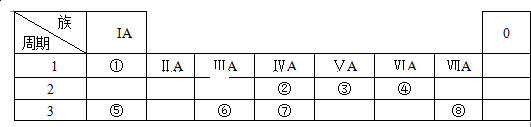
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③④⑤⑥ | B. | ②③⑤ | C. | ①②④⑤ | D. | ①③⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com