
A、B、C、D、E是中学常见的5种化合物,A、B是氧化物,元素X、Y的单质是生活中常见的金属,相关物质间的关系如图所示。

(1)X的单质与A反应的化学方程式是 。
(2)若试剂1是NaOH溶液,X的单质与试剂1反应的离子方程式是 。
(3)若试剂1和试剂2均是稀硫酸。
①检验物质D的溶液中金属离子的方法是 。
②将物质C溶于水,其溶液呈酸性,原因是(用离子方程式表示) 。
③某高效净水剂是由Y(OH)SO4聚合得到的。工业上以E、稀硫酸和亚硝酸钠为原料来制备Y(OH)SO4,反应中有NO生成,该反应的化学方程式是 。
(1)金属与金属氧化物之间可发生置换反应主要是铝与高熔点金属氧化物发生铝热反应,故X为铝,作为生活中常见金属,Y为铁,A、B分别为三氧化二铁和三氧化二铝。铝与三氧化二铁发生铝热反应的化学方程式为

(2)若试剂1是NaOH溶液,则离子反应方程式为2Al+2H2O+2OH-====2Al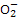 +3H2↑。
+3H2↑。
(3)若试剂1和试剂2均是稀硫酸,则C、D、E分别是硫酸铝、硫酸铁、硫酸亚铁。
①检验Fe3+的方法是向溶液中加入KSCN溶液,看溶液是否显红色。
②硫酸铝溶液中铝离子水解显酸性,离子方程式为Al3++3H2O Al(OH)3+3H+
Al(OH)3+3H+
③工业上以FeSO4、稀硫酸和亚硝酸钠为原料来制备Fe(OH)SO4,亚硝酸钠还原为NO,Fe2+氧化为Fe3+,化学反应方程式为
2FeSO4+2NaNO2+H2SO4====2Fe(OH)SO4+Na2SO4+2NO↑。
答案:(1)
(2)2Al+2H2O+2OH-====2Al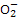 +3H2↑
+3H2↑
(3)①取少量溶液于试管中,滴加KSCN溶液,溶液变红色则证明原溶液中含有Fe3+
②Al3++3H2O Al(OH)3+3H+
Al(OH)3+3H+
③2FeSO4+2NaNO2+H2SO4====2Fe(OH)SO4+Na2SO4+2NO↑


科目:高中化学 来源: 题型:
合成氨的温度和压强通常控制在约500℃以及20 MPa~50 MPa的范围,当进入合成塔的N2和H2的体积比为1∶3时,经科学实验测定,在相应条件下N2和H2反应所得氨的平衡浓度(体积分数)如下表所示:

而实际上从合成塔出来的混合气体中含有氨约为15%。
请回答下列问题:
(1)298 K下合成氨时,每生成1 mol 氨气,同时放出46.2 kJ的热量,则该反应的热化学方程式为_________________________________________________。
氨气,同时放出46.2 kJ的热量,则该反应的热化学方程式为_________________________________________________。
在该温度下,取1 mol N2和3 mol H2放在一密闭容器中,在催化剂存在的条件下进行反应,测得反应放出的热量总小于92.4 kJ,其原因是______________。
(2)实际上从合成塔出来的混合气体中氨的体积分数小于理论值的根本原因是_______________。
A.表中所测数据有明显误差
B.生产条件控制不当
C.氨的分解速率大于预测值
D.合成塔中的反应未达到平衡状态
(3)若工业生产中N2和H2按投料比1∶2.8的比例进入合成塔,那么转化率较大的应该是_________,采用此投料比的原因是______________,
若从合成塔出来的混合气体中氨的体积分数仍为15%,则N2和H2的转化率之比是__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
宋代著名法医学家宋慈的《洗冤集录》中有“银针验毒”的记载,“银针验毒”的原理是4Ag+2H2S+O2====2X+2H2O,下列说法中正确的是( )
A.X的化学式为AgS
B.银针验毒时,空气中氧气失去电子
C.反应中Ag和H2S均是还原剂
D.每生成1 mol X,反应转移2 mol电子
查看答案和解析>>
科目:高中化学 来源: 题型:
可逆反应aA(g)+bB(g)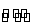 cC(g)+dD(g),取a mol A和b mol B置于V L容器中,1 min后,测得容器内A的浓度为x mol·L-1。
cC(g)+dD(g),取a mol A和b mol B置于V L容器中,1 min后,测得容器内A的浓度为x mol·L-1。
(1)此时C的浓度为 _________mol·L-1。
(2)D的物质 的量为_________mol。
的量为_________mol。
(3)这段时间内反应的平均速率若以物质A的浓度变化来表示,应为__________。
(4)B的转化率为_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
向10 mL 0.1 mol·L-1NH4Al(SO4)2溶液中,滴加等浓度Ba(OH)2溶液xmL,下列叙述正确的是( )
A.x=10时,溶液中有N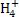 、Al
、Al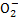 、S
、S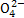 ,且c(N
,且c(N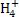 )>c(S
)>c(S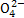 )
)
B.x=10时,溶液中有N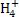 、Al3+、S
、Al3+、S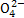 ,且c(N
,且c(N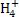 )>c(Al3+)
)>c(Al3+)
C.x=30时,溶液中有Ba2+、Al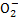 、OH-,且c(OH-)<c(Al
、OH-,且c(OH-)<c(Al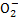 )
)
D.x=30时,溶液中有Ba2+、Al3+、Al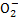 ,且c(OH-)=c(Ba2+)
,且c(OH-)=c(Ba2+)
查看答案和解析>>
科目:高中化学 来源: 题型:
如图装置中,小试管内为红墨水,具支试管内盛有pH=4的雨水和生铁片。观察:开始导管内液面下降,一段时间后导管内液面回升,略高于小试管液面。以下有关解释合理的是( )
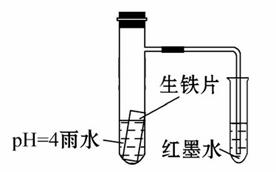
A.生铁片中的碳是原 电池的阳极,发生还原反应
电池的阳极,发生还原反应
B.雨水酸性较强,生铁片仅发生析氢腐蚀
C.墨水回升时,碳极反应式为:O2+2H2O+4e-====4OH-
D.具支试管中溶液pH逐渐减小
查看答案和解析>>
科目:高中化学 来源: 题型:
根据下列事实得出的结论正确的是( )
A.Na2SO3试样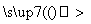
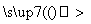 白色沉淀
白色沉淀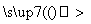 沉淀不溶解 结论:此Na2SO3试样已变质
沉淀不溶解 结论:此Na2SO3试样已变质
B.稀硫酸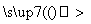 产生气泡的速率较慢
产生气泡的速率较慢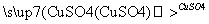 产生气泡的速率明显加快 结论:CuSO4对此反应有催化作用
产生气泡的速率明显加快 结论:CuSO4对此反应有催化作用
C.某溶液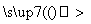 瓶口产生白雾
瓶口产生白雾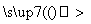 瓶口产生白烟 结论:此溶液一定为浓盐酸
瓶口产生白烟 结论:此溶液一定为浓盐酸
D.无色试液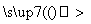 产生无色无味气体
产生无色无味气体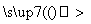 石灰水变浑浊 结论:原无色试液中可能含有CO
石灰水变浑浊 结论:原无色试液中可能含有CO
查看答案和解析>>
科目:高中化学 来源: 题型:
化学与社会、生活密切相关,下列说法正确的是( )
A.制作航天服的聚酯纤维和用于光缆通信的光导纤维都是新型无机非金属材料
B.淀粉、明矾属于纯净物,矿泉水、食醋属于混合物
C.丁达尔现象可用于区别溶液与胶体,云、雾、稀硫酸均能产生丁达尔现象
D.“地沟油”经过加工处理制得肥皂或生物柴油,可以实现厨余物合理利用
查看答案和解析>>
科目:高中化学 来源: 题型:
在中学化学实验中使用的玻璃、陶瓷等仪器,在实验操作中不能承受温度的急剧变化,否则会引起安全事故。下列实验操作过程不是基于上述原因的是( )
A.钠与水反应时,只能取黄豆粒大小的钠投入盛水的烧杯中反应
B.在用二氧化锰和浓盐酸制氯气时,在加入二氧化锰后应首先加入浓盐酸,然后再点燃酒精灯
C.在用固体氯化铵和氢氧化钙制取氨气结束后,将大试管从铁架台上取下置于石棉网上冷却后再洗涤
D.用排水法收集气体后,先移出导气管,后熄灭酒精灯
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com