
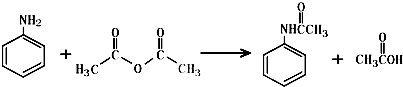
分析 (1)研碎后使反应物之间充分接触,以便充分反应,提高反应产率;从影响化学反应速率的因素方面进行分析,如减小反应物浓度可以降低反应速率;
(2)根据题中信息“苯胺微溶于冷水;纯乙酰苯胺是无色片状晶体,不溶于冷水,可溶于热水;乙酸酐遇水缓慢反应生成乙酸”分析选用的洗涤试剂;
(3)根据题干信息,过滤Ⅰ需要趁热过滤,避免温度降低导致产物析出,影响产率;加入过量的水的目的主要是避免溶剂的损失、温度的降低可能导致产物析出,影响产率;
(4)抽滤时,颗粒太小会在滤纸上形成一层密实的沉淀,溶液不易透过,抽滤速度慢;
(5)根据实验操作对产物乙酰苯胺的量影响进行解答,如①②③的存在都可以降低乙酰苯胺的损失,而④不影响产率、⑤会降低产率;
(6)根据题中数据计算出苯胺、乙酸酐的物质的量,然后根据不足量计算出生成乙酰苯胺的物质的量,再根据实际上生成的乙酰苯胺的质量计算出产率.
解答 解:(1)若有结块现象产生,反应物可能被产物包裹,反应不能充分,影响了产率,所以步骤①研碎块状产物的目的为:防止原料被产物包裹,使之充分反应,提高产率;
A.反应快结束时的充分搅拌,使反应更完全,无法降低反应速率,可能会导致反应速率加快,温度升高,故A错误;
B.旋摇下分批加入6.0mL乙酸酐,使反应物浓度较小,反应速率较慢,从而降低了反应温度,故B正确;
C.玻璃棒将块状物研碎,目的是防止原料被产物包裹,使之充分反应,不利于控制温度,故C错误;
D.加20mL水,可以使溶液稀释,降低反应速率,还可以使溶液质量增大,从而降低了温度,故D正确;
故答案为:防止原料被产物包裹,使之充分反应,提高产率;BD;
(2)苯胺微溶于冷水,而纯乙酰苯胺不溶于冷水,可溶于热水,且乙酸酐遇水缓慢反应生成乙酸,所以可用冷水洗涤粗产品乙酰苯胺,从而除去含有的杂质苯胺和乙酸酐,所以B正确,
故答案为:B;
(3)根据步骤③操作方法可知,由于乙酰苯胺的溶解度受温度影响较大,为了避免温度降低析出乙酰苯胺,所以需要趁热过滤;加入过量的水的,可以避免在操作过程中因溶剂的损失或温度的降低析出产物,影响产率,与活性炭的吸附性无关,所以AB正确,
故答案为:趁热过滤;AB;
(4)抽滤时,颗粒太小会在滤纸上形成一层密实的沉淀,溶液不易透过,抽滤速度慢,
故答案为:沉淀颗粒太小则易在滤纸上形成一层密实的沉淀,溶液不易透过;
(5)①配制成饱和溶液后,加入过量20%的溶剂,可以防止后续过程中,溶剂损失、温度降低可能导致的产物析出,有利于提高产率;
②趁热过滤近沸溶液,乙酰苯胺的溶解度受温度影响较大,较高温度下可以减少在过滤过程中导致产物减少,有利于提高产率;
③过滤Ⅰ时用少量沸水淋洗烧杯和漏斗中的固体,合并滤液,避免烧杯和漏斗中有残留的产物,可以提高产;
④加活性炭吸附,需要吸附有色物质,无法提高产率;
⑤过滤Ⅱ时的洗涤选用热水代替冷水洗涤固体,导致乙酰苯胺的溶解度增大,损失的乙酰苯胺较多,降低了产率;
根据以上分析可知,可以通过产率的有:①②③;不能提高产率的为:④⑤,所以C正确,
故答案为:C;
(6)5.0mL苯胺(密度1.04g/mL)的物质的量为:$\frac{1.04g/mL×5.0mL}{93g/mol}$≈0.056mol,
6.0mL乙酸酐(密度1.08g/mL)的物质的量为:$\frac{1.08g/mL×6.0mL}{102g/mL}$≈0.064mol,
乙酸酐过量,理论上反应生成乙酰苯胺的物质的量为0.056mol,
则该实验乙酰苯胺的产率为:$\frac{6.75g}{135g/mol×0.056mol}$×100%≈89%,
故答案为:89%.
点评 本题通过用苯胺与乙酸酐为原料制取和提纯乙酰苯胺,考查了化学实验方案的设计方法,题目难度较大,试题知识点较多、综合性较强,明确制备原理为解答关键,试题充分考查了学生的分析、理解能力及化学实验能力.


科目:高中化学 来源: 题型:选择题
| A. | 同一周期中,碱金属元素的第一电离能最大 | |
| B. | 同周期元素中,ⅦA族元素的原子半径最大 | |
| C. | 当各轨道处于全满、半满、全空时原子较稳定 | |
| D. | ⅥA族元素的原子,其半径越大,越容易得到电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验操作 | 实验目的或结论 |
| A | 当溶液发生过饱和现象时,用玻璃棒轻轻摩擦器壁. | 促使晶体析出 |
| B | 将一块擦去氧化膜的铝片放在浓硝酸中,一段时间后取出洗净,再放入一定浓度的CuSO4溶液中. | 验证Al在浓硝酸中的钝化 |
| C | 在食醋总酸含量测定实验中,用25mL移液管吸取市售食醋25mL,置于250mL容量瓶中,加水稀释至刻度线,摇匀得待测食醋溶液 | 主要是防止食醋的挥发而导致实验误差. |
| D | 把两根碳棒放在酒精喷灯火焰上灼烧2~3分钟后,立即投入到冷水中,反复操作3~5次. | 可以使碳棒表面变得粗糙多孔,便于吸收更多的气体 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 摘下几根火柴头,浸于水中,片刻后取少量溶液于试管中,加AgNO3溶液、稀硝酸,若出现白色沉淀,说明含氯元素 | |
| B. | 纸层析法分离叶绿素a和叶绿素b时,若点样的斑点太大,则会导致色谱分离不清 | |
| C. | 在抽滤装置中洗涤沉淀时,应关小水龙头,使洗涤剂缓慢通过沉淀物 | |
| D. | 在Zn-Cu原电池中加入高锰酸钾、双氧水等强氧化剂,灯泡亮度增加且持续时间较长 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 .
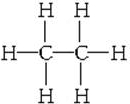
.
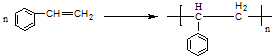 .
.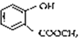 含有的官能团的名称为酚羟基、酯基.
含有的官能团的名称为酚羟基、酯基.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 三种元素对应的氧化物均为碱性氧化物 | |
| B. | 三者的单质长期放置在空气中均能被腐蚀 | |
| C. | 制备AlCl3、FeCl3、CuCl2均不能采用将溶液直接蒸干的方法 | |
| D. | 电解AlCl3、FeCl3、CuCl2的混合溶液时,阴极上依次析出Cu、Fe、Al |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将金属钠投入水中:Na+2H2O═Na++OH-+H2↑ | |
| B. | 过量CO2通人Ca(ClO)2溶液中:ClO-+CO2+H2O═HCO3-+HCIO | |
| C. | NH4HCO3溶液与过量的NaOH溶液反应:NH4++OH-═NH3↑+H2O | |
| D. | 铜片溶于稀硝酸中:Cu+4H++2NO3-═Cu2++2NO2↑+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com