
 有A、B、C、D、E五种元素.其相关信息如下:
有A、B、C、D、E五种元素.其相关信息如下:| 元素 | 相关信息 |
| A | A元素的一种原子没有中子,只有一个质子 |
| B | B是电负性最大的元素 |
| C | C的基态原子2p轨道有三个未成对电子 |
| D | D为主族元素,且与E同周期,其最外层上有两个运动状态不同的电子 |
| E | E能形成砖红色(红色)的E2O和EO两种氧化物 |
分析 A元素的一种原子没有中子,只有一个质子,则A是H元素;
B是电负性最大的元素,则为F元素;
C的基态原子2p轨道有三个未成对电子,为N元素;
E能形成砖红色(红色)的E2O和EO两种氧化物,则E为Cu元素;
D为主族元素,且与E同周期,其最外层上有两个运动状态不同的电子,说明其最外层上有两个电子,为Ca元素;
(1)E为Cu元素,其M层有18个电子,分别位于3s、3p、3d能级上,根据构造原理书写;
(2)C是N元素,其单质为N2,氮气分子中存在氮氮三键,三键中含有1个δ键和2个π键;
(3)含有氢键的物质熔沸点较高;根据价层电子对互斥理论确定原子杂化类型;
(4)含有空轨道和含有孤电子对的原子之间存在配位键,不同非金属元素之间易形成极性键;平面正方形结构的二元氯代物有两种结构;
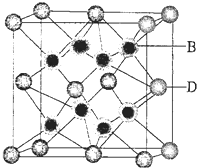
(5)根据图知,D离子配位数是8;根据密度公式ρ=$\frac{m}{V}$计算晶胞中距离最近的B和D之间的距离.
解答 解:A元素的一种原子没有中子,只有一个质子,则A是H元素;
B是电负性最大的元素,则为F元素;
C的基态原子2p轨道有三个未成对电子,为N元素;
E能形成砖红色(红色)的E2O和EO两种氧化物,则E为Cu元素;
D为主族元素,且与E同周期,其最外层上有两个运动状态不同的电子,说明其最外层上有两个电子,为Ca元素;
(1)E为Cu元素,其M层有18个电子,分别位于3s、3p、3d能级上,根据构造原理知,其排布式为3s23p63d10,
故答案为:3s23p63d10 ;
(2)C是N元素,其单质为N2,氮气分子中存在氮氮三键,三键中含有1个δ键和2个π键,则C元素单质分子中含有δ和π键的键数之比为1:2,故答案为:l:2;
(3)乙醇中的羟基与水的羟基结构相似所以溶解度大,C7H15OH中烃基大,与水的羟基结构相似程度小所以溶解度小,N2H4分子每个N原子含有3个共价单键和1个孤电子对,所以N原子采用sp3杂化,
故答案为:乙醇中的羟基与水的羟基结构相似所以溶解度大,C7H15OH中烃基大,与水的羟基结构相似程度小所以溶解度小;sp3;
(4)Cu(NH3)42+配离子中Cu原子和N原子之间存在配位键、N-H原子之间存在极性键,故选①③;
若 Cu(NH3)42+具有对称的空间构型,且当 Cu(NH3)42+中的两个NH3分子被两个Cl取代时.能得到两种不同结构的产物,则 Cu(NH3)42+空间构型为平面正方形;
故答案为:①③;a;
(5)根据图片知,每个D原子连接8个B原子,所以D原子配位数是8,
该晶胞中氟离子个数为8,钙离子个数=8×$\frac{1}{8}$+6×$\frac{1}{2}$=4,ρ=$\frac{m}{V}$=$\frac{\frac{M}{{N}_{A}}×4}{V}$则V=$\frac{\frac{M}{{N}_{A}}×4}{ρ}$=$\frac{78×4}{ρ{N}_{A}}$,
该晶胞中四个钙离子形成正四面体结构,氟离子位于正四面体的体心上,其图象为: ,
,
晶胞边长=$\root{3}{\frac{78×4}{ρ{N}_{A}}}$cm,正四面体棱长=$\frac{\sqrt{2}}{2}$×$\root{3}{\frac{78×4}{ρ{N}_{A}}}$cm,
在正三角形BCD中BE的长=$\frac{\sqrt{3}}{2}$×$\frac{\sqrt{2}}{2}$×$\root{3}{\frac{78×4}{ρ{N}_{A}}}$cm,BO与OE的长之比为2:1,则BO的长=$\frac{2}{3}$×$\frac{\sqrt{3}}{2}$×$\frac{\sqrt{2}}{2}$×$\root{3}{\frac{78×4}{ρ{N}_{A}}}$=$\frac{\sqrt{6}}{6}×\root{3}{\frac{78×4}{ρ{N}_{A}}}$cm,
(AO的边长)2=($\frac{\sqrt{2}}{2}$×$\root{3}{\frac{78×4}{ρ{N}_{A}}}$)2-($\frac{\sqrt{6}}{6}×\root{3}{\frac{78×4}{ρ{N}_{A}}}$)2,
设氟离子和钙离子的边长为x,
x2=($\frac{\sqrt{6}}{6}×\root{3}{\frac{78×4}{ρ{N}_{A}}}$)2-(AO的边长-x)2,x=$\frac{\sqrt{3}}{4}$×$\root{3}{\frac{78×4}{ρ{N}_{A}}}$,
故答案为:8;$\frac{\sqrt{3}}{4}$×$\root{3}{\frac{78×4}{ρ{N}_{A}}}$.
点评 本题考查较综合,涉及晶胞计算、微粒构型判断、原子核外电子排布等知识点,同时考查学生空间想象能力、计算能力,难点是晶胞计算,明确正四面体中顶点到中心的距离及中心到底面距离的比是解本题关键,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 多植树造林,严禁乱砍滥伐 | B. | 使用新能源,减少煤炭使用 | ||
| C. | 少开私家车,控制尾气排放 | D. | 杜绝浪费,实施“光盘行动” |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 5n-2 | B. | 12-3n | C. | 3n-12 | D. | 3n-6 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②③⑤ | B. | ②③⑤⑥ | C. | ②⑤⑥ | D. | ①② |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 5种 | B. | 6种 | C. | 7种 | D. | 8种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | I和Ⅱ的物质的量浓度均为0.001mol•L-1 | |
| B. | 将I稀释10倍,溶液中 c(CH3COOH)、c(OHˉ)均减小 | |
| C. | I和Ⅱ溶液混合,若c(OH-)>c(H+),则氢氧化钠过量 | |
| D. | I和Ⅱ等体积混合后,溶液中离子浓度大小为c(CH3COO-)>c(Na+)>c(H+)>c(OH--) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
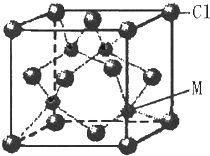 已知W、X、Y、Z、R五种元素是短周期的元素,原子序数依次增大,其中X 的基态原子中成对的电子的对数与单个电子的数目相同,Y 是地壳中含量最多的元素,R的单质是淡黄色固体,不溶于水,能溶于CS2.在短周期中:W的原子半径最小,Z 的原子半径最大.又知M是第四周期的元素,M的最外层只有一个单电子,次外层的轨道上全部填充满了电子.
已知W、X、Y、Z、R五种元素是短周期的元素,原子序数依次增大,其中X 的基态原子中成对的电子的对数与单个电子的数目相同,Y 是地壳中含量最多的元素,R的单质是淡黄色固体,不溶于水,能溶于CS2.在短周期中:W的原子半径最小,Z 的原子半径最大.又知M是第四周期的元素,M的最外层只有一个单电子,次外层的轨道上全部填充满了电子.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用碱石灰干燥氨气 | |
| B. | 用紫色石蕊试液检验酸性溶液 | |
| C. | 通入Cl2除去FeCl3溶液中的FeCl2 | |
| D. | 加入Fe粉除去Al3+溶液中的杂质Cu2+ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com