
| A. | CO为氧化产物,H2为还原产物 | B. | CaCN2含有共价键,属于共价化合物 | ||
| C. | HCN既是氧化剂又是还原剂 | D. | 每消耗10g CaCO3生成2.24L CO2 |
分析 在CaCO3+2HCN=CaCN2+CO↑+H2↑+CO2↑反应中,HCN中的碳元素化合价由+2升高到+4,对应的氧化产物为CaCN2,HCN中的氢元素化合价由+1价降低到0,对应的还原产物为H2,以此解答该题.
解答 解:A.CO由HCN生成,既不是氧化产物也不是还原产物,故A错误;
B.CaCN2中存在[N=C=N]2-,含有离子键和共价键,属于离子化合物,故B错误;
C.因HCN中的碳元素化合价升高,氢元素的化合价降低,则HCN既是氧化剂又是还原剂,故C正确;
D.气体存在的条件未知,不能确定体积大小,故D错误.
故选C.
点评 本题考查氧化还原反应,为高频考点,侧重于学生的分析能力的考查,注意利用元素的化合价来分析氧化还原反应,明确反应中各物质中的元素的化合价是解答的关键,本题的难点是氧化产物的分析.


科目:高中化学 来源: 题型:选择题
| 实验操作 | 现象 | 解释或结论 |
| 在稀硝酸中加入过量的铁粉,充分反应后滴入KSCN溶液 | 溶液呈红色 | HNO3将Fe氧化为Fe3+ |
| AgI沉淀中滴入KCl溶液 | 有白色沉淀出现 | AgCl比AgI更难溶 |
| Cl2通入品红溶液中 | 溶液褪色 | Cl2具有漂白性 |
| 用玻璃棒蘸取浓氨水点到红色石蕊试纸上 | 试纸变蓝色 | 浓氨水呈碱性 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C5H10和C6H6 | B. | C2H6和C2H4O2 | C. | C3H6和C3H8 | D. | C2H6和C3H8 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 A、B、C、D、E、F是元素周期表中前四周期的元素,原子序数依次增大,A、B是相邻的同一短周期元素,其中A元素所形成的化合物种类最多.C、D、E、F是位于同一周期的金属元素,基态C、F原子的价电子层中未成对电子均为1个,且C、F原子的电子数目相差10.基态D、E原子的价电子层中未成对电子数分别为4、2.且原子序数相差2,其中D元素是生产、生活中常见的金属.
A、B、C、D、E、F是元素周期表中前四周期的元素,原子序数依次增大,A、B是相邻的同一短周期元素,其中A元素所形成的化合物种类最多.C、D、E、F是位于同一周期的金属元素,基态C、F原子的价电子层中未成对电子均为1个,且C、F原子的电子数目相差10.基态D、E原子的价电子层中未成对电子数分别为4、2.且原子序数相差2,其中D元素是生产、生活中常见的金属.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该转化过程是物理变化 | |
| B. | 1molCO2原子晶体中含2molC-O键 | |
| C. | CO2原子晶体的熔点高于SiO2 | |
| D. | CO2的原子晶体和分子晶体互为同分异构体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. |  制取纯净氢氧化亚铁 | B. | 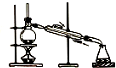 石油的蒸馏 | ||
| C. | 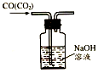 除去CO气体中的CO2气体 | D. | 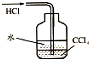 吸收HCl |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
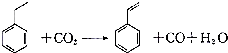
| A. | 分子中含有5个碳碳双键 | B. | 属于不含极性键的共价化合物 | ||
| C. | 分子式为C8H10 | D. | 通过加聚反应生成聚苯乙烯 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaCl | B. | KOH | C. | Al2O3 | D. | MgSO4溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com