
【题目】近年来食品安全问题成为社会各界日益关注的焦点话题.香港地区食环署食物安全中心曾对十五个桂花鱼样本进行化验,结果发现十一个样本中含有孔雀石绿。孔雀石绿是化工产品,具有较高毒性,高残留,且长期服用后,容易致癌、致畸,对人体有害。其结构简式如图所示。下列关于孔雀石绿的说法正确的是( )

A.孔雀石绿的分子式为C23H25N2
B.1mol孔雀石绿在一定条件下最多可与6molH2发生加成反应
C.孔雀石绿属于芳香烃
D.孔雀石绿苯环上的一氯取代物有5种
【答案】D
【解析】
A. 根据结构式确定分子式;
B. 孔雀石绿中含有2个苯环和3个碳碳双键,均可与H2发生加成反应;
C. 含有苯环的烃为芳香烃;
D. 有机物中含有2个苯环,根据结构对称进行分析。
A. 根据结构式可知孔雀石绿的分子式为C23H26N2,A项错误;
B. 孔雀石绿中含有2个苯环和3个碳碳双键,均可与H2发生加成反应,因此1mol孔雀石绿在一定条件下最多可与9molH2发生加成反应,B项错误;
C. 孔雀石绿不是烃,除了C、H两种元素外还含有N,属于芳香族化合物,但不是芳香烃,C项错误;
D. 有机物中含有2个苯环,左下角苯环中含有2种不同环境的氢原子,上方的苯环有3种不同环境的氢原子,因此苯环上的一氯取代物有5种,D项正确;
答案选D。


科目:高中化学 来源: 题型:
【题目】某温度下,体积和pH都相同的盐酸和氯化铵溶液加水稀释时的pH变化曲线如下图所示,下列判断正确的是
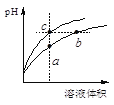
A.a、c两点溶液的导电能力相同
B.b点溶液中c(H+)+c(NH3·H2O)=c(OH-)
C.a、b、c三点溶液水的电离程度a>b>c
D.与等体积b、c处溶液反应,消耗等量的NaOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关物质的量的计算是中学化学的重要部分,请回答下列有关物质的量的计算问题。
(1)等质量的O2和O3所含分子个数比为________,所含原子个数比为_______。
(2)设NA为阿伏加德罗常数的数值,如果a g氧气中含有的分子数为b,则c g氧气在标准状况下的体积约是__________(用含NA的式子表示)。
(3)在同温、同压下,实验测得CO、N2和O2三种气体的混合气体的密度是H2的14.5倍,若其中CO和N2的物质的量之比为1∶1,则混合气体中氧元素的质量分数为__________。
(4)标准状况下,将V L A气体(摩尔质量为M g/mol)完全溶于0.1 L水(密度1 g/cm3)中,所得溶液的密度为d g/mL,则此溶液的物质的量浓度为_______mol/L。
(5)100mL0.3mol/LNa2SO4溶液和50mL0.2mol/LAl2(SO4)3溶液混合后(溶液体积保持不变),溶液中SO42-的物质的量浓度为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】相同温度下,容积相同的甲、乙两个恒容密闭容器中均发生如下反应:2SO2(g)+O2(g) ![]() 2SO3(g) △H=-197 kJ/mol ,实验测得有关数据如下:
2SO3(g) △H=-197 kJ/mol ,实验测得有关数据如下:
容器编号 | 起始时各物质的物质的量 / mol | 达到平衡时体系能量的变化/kJ | ||
SO2 | O2 | SO3 | ||
甲 | 2 | 1 | 0 | 放出热量:Q1 |
乙 | 1.8 | 0.9 | 0.2 | 放出热量:Q2 |
下列判断中正确的是
A.两容器中反应的平衡常数不相等
B.达到平衡时SO2的体积分数:甲<乙
C.197>Q1>Q2
D.生成1molSO3(l)时放出的热量等于98.5kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组同学在查阅资料的基础上对乙醛与新制氢氧化铜的反应进行了探究。
(1)乙醛与新制氢氧化铜反应的化学方程式为________。
(查阅资料)i.乙醛在碱性条件下可发生缩合等反应生成有色物质;ii.溶液的酸碱性可能会影响物质的氧化性、还原性。
(初步探究)
序号 | 实验操作 | 实验现象 |
I | 向试管中加入4 mL 10 % NaOH溶液,滴入0.5 mL 水,加入0.5 mL 40 %乙醛溶液,振荡;在酒精灯上加热至沸腾后保持沸腾 | 无色溶液逐渐变黄,并变浑浊;加热后得黄色浊液,之后无明显变化 |
II | 向试管中加入4 mL 10 % NaOH溶液,滴入0.5 mL 2 %CuSO4溶液,振荡;加入0.5 mL 40 %乙醛溶液,振荡;在酒精灯上加热至沸腾后保持沸腾 | 蓝色浊液依次呈绿色、黄色、橙色,最终生成红色固体;之后无明显变化 |
III | 向试管中加入4 mL水,滴入0.5 mL 2 %CuSO4溶液,振荡;加入0.5 mL 40 %乙醛溶液,振荡;在酒精灯上加热至沸腾后保持沸腾 | 蓝色溶液无明显变化 |
(2)实验I的目的是________。
(3)甲同学为了检验实验II中红色固体的成分进行了如下实验:取少量红色固体于试管中,加入适量稀HNO3,振荡,观察到红色固体完全溶解,得蓝色溶液。甲同学认为,该实验现象说明实验II中反应生成了Cu。乙同学认为甲的观点不正确,理由是_____。
(深入探究)乙同学对比实验II和实验III,对实验II能够发生反应的原因提出了猜想:乙醛的还原性随着溶液碱性的增强而增强,并利用实验IV进行验证。
实验装置 | 序号 | A池试剂 | B池试剂 | 实验现象 |
| IV-1 | 0.2% CuSO4溶液 | Na2SO4溶液和40%乙醛溶液按体积比9:1混合 | 指针不偏转,A、B池中均无明显变化 |
IV-2 | 0.2% CuSO4溶液 |
(4)实验IV-1中,Na2SO4溶液的作用是________。
(5)实验IV-2中,B池中的试剂是________。
(6)根据实验现象,乙同学认为其猜想成立。乙同学观察到的实验现象是________。
(7)综合上述实验,小组同学经过深入讨论,认为除了乙同学的猜想外,与实验III相比,实验II能够发生反应的原因还可能有________和________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列大小关系正确的是
A.熔点:己烷>2-甲基丁烷>戊烷>丁烷
B.含氢量:甲烷>乙烷>乙烯>乙炔>苯
C.密度:苯>H2O>CCl4
D.相同物质的量物质完全燃烧耗氧量:己烷>环己烷>苯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关系正确的是( )
A. 沸点:戊烷>2,2-二甲基戊烷>2,3-二甲基丁烷>丙烷
B. 密度:CCl4>CHCl3>H2O>苯
C. 含氢质量分数:甲烷>乙烷>乙烯>乙炔>苯
D. 等质量的物质燃烧耗O2量:苯>乙烷>乙烯>甲烷
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质:①铜片 ②![]() ③
③![]() ④
④![]() ⑤
⑤![]() ⑥
⑥![]() ⑦
⑦![]() ⑧氨水。
⑧氨水。
(1)把上述各物质按物质分类方法填写在下表的空白处(填物质编号)
分类标准 | 碱性氧化物 | 非电解质 | 弱酸 |
属于该类的物质 | ___________ | ___________ | ______________ |
(2)把上述各物质按物质分类方法填写在下表的空白处(填物质编号)。
(3)在标准状况下,相同体积的②和④,其原子个数比为_________。
(4)写出氢氧化钡的电离方程式:______________。
(5)上述物质中有两种物质之间可发生离子反应:![]() ,该离子反应对应的化学方程式为:______________。
,该离子反应对应的化学方程式为:______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com