
取50.0mL K2CO3和K2SO4的混合溶液,加入过量BaCl2溶液后得到12.18g白色沉淀,用过量稀硝酸处理后沉淀量减少到2.33g,并有气体放出(忽略溶液体积的变化)。试计算:(请写出计算过程)
(1)原混合溶液中K2CO3和K2SO4的物质的量浓度。
(2)产生的气体在标准状况下的体积。
科目:高中化学 来源: 题型:
(1) 在标准状况下,测得1.32 g某气体的体积为0.672 L。则此气体的摩尔质量为 。
(2)等质量CO、CO2两种气体的的摩尔质量之比为 ;同温同压下的体积比为 ;其中氧元素的原子个数比为 。
(3)常用食醋除去水壶中的水垢,以氢氧化镁为例,表明反应原理(用离子方程式表示):
。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列反应中,SO2作还原剂的是( )
|
| A. | 2H2S+SO2→3S↓+2H2O | B. | SO2+2Mg→2MgO+S |
|
| C. | Cl2+SO2+2H2O→H2SO4+2HCl | D. | SO2+2NaOH→Na2SO3+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
某溶液中滴入BaCl2溶液,产生白色沉淀,再滴入稀硝酸,沉淀不溶解,则该溶液中:( )
A.一定有SO42- B.SO42-、 SO32-或Ag+ 中至少有一种
C.一定无Ag+ D.可能有CO32-
查看答案和解析>>
科目:高中化学 来源: 题型:
下图是中学化学中常用于混合物的分离和提纯的装置,请根据装置回答问题:
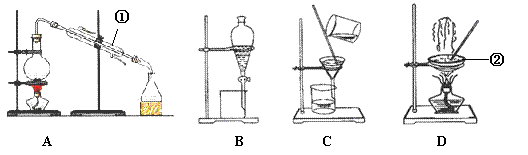
(1)从氯化钾溶液中得到氯化钾固体,选择装置________(填代表装置图的字母,下同);除去自来水中的Cl- 等杂质,选择装置__________。
(2)从碘水中分离出I2,选择装置 ,该分离方法的名称为 。
(3)装置A中①的名称是 ,装置D中②的名称是 。
(4)装置B在分液时为使液体顺利滴下,应进行的具体操作是____________________ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组离子能在溶液中大量共存的是( )。
A.Ag+、K+、NO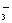 、Cl- B.Mg2+、Na+、Cl-、SO
、Cl- B.Mg2+、Na+、Cl-、SO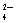
C.Ca2+、Mg2+、OH-、Cl- D.H+、Na+、CO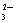 、SO
、SO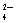
查看答案和解析>>
科目:高中化学 来源: 题型:
某无色透明溶液中可能含有Na+、Ba2+、Cu2+、CO32-、Cl–、Mg2+中的一种或几种离子。
①向此溶液中滴加稀盐酸无明显现像。
②取少许①的溶液并加入少量的Na2SO4溶液,有白色沉淀产生。
③取②的上层清液并加入过量的NaOH溶液,无明显现象。
(1)原溶液中除了有Cl–外还一定含有的离子是 ,一定不含的离子是 ,不能确定是否含有的离子时 。
(2)②中反应的离子方程式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
某溶液中含有0.2mol/L NH4+、0.25mol/L Fe2+、0.4mol/L Cl-及一定量的SO4 2-,则SO4 2-的物质的量浓度为
A. 0.5mol/L B. 0.3mol/L C. 0.15mol/L D. 0.1mol/L
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com