
【题目】如图Ⅰ、Ⅱ、Ⅲ是常见的气体发生装置;V、VI是气体收集装置,根据要求回求答下列问题: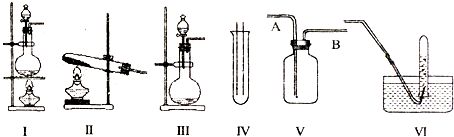
(1)气体发生装置的选择:若用CaCO3与盐酸反应制CO2 , 则可选择;(填序号)若用I装置制取氯气,则浓盐酸应盛放在(填I中的仪器名称).写出实验室制取氯气的化学方程式 .
(2)收集装置的选择:若选用V为氯气收集装置,则氯气应从口通入.用化学方法检验氯气收集满的方法是 .
(3)实验室制取氯气,多余的氯气要进行尾气处理,一般将尾气通入到溶液中,其发生反应的化学方程式为 .
(4)气体的吸收:若经试验发现,现1体积的水已吸收336体积的HCl,且得到的溶液的密度为1.08g/cm3 , 则所得溶液中溶质的物质的量浓度为mol/L.(保留一位小数)
【答案】
(1)Ⅲ,分液漏斗,MnO2+4HCl(浓) ![]() MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
(2)A,将湿润的淀粉KI试纸放在B口处,试纸变蓝色,证明氯气已集满
(3)NaOH溶液,2NaOH+Cl2=NaCl+NaClO+H2O
(4)10.5
【解析】解:(1)若用CaCO3与盐酸反应制CO2,为固体和液体的反应,常温下可进行,可选择Ⅲ装置,用I装置制取氯气,浓盐酸放在分液漏斗中,浓盐酸和二氧化锰在加热条件下反应生成氯气、氯化锰和水,反应的方程式为:MnO2+4HCl(浓) ![]() MnCl2+Cl2↑+2H2O;
MnCl2+Cl2↑+2H2O;
(2)氯气的密度大于空气的密度,所以应采用向上排空气法收集氯气,故A为进气口;氯气的氧化性大于碘的氧化性,所以氯气能置换出碘化钾中的碘,且碘遇淀粉变蓝色,所以可用湿润的淀粉KI试纸检验是否收集满了氯气.
(3)氯气有毒,逸出会污染大气,所以不能让氯气逸出;氯气和水能反应是盐酸和次氯酸,盐酸和次氯酸是酸,都能和碱反应,所以可用氢氧化钠溶液吸收氯气;
(4)1体积的水已吸收336体积的HCl,可设水的体积为1L,HCl的体积为336L,则标准状况下336L HCl的物质的量为: ![]() =15mol,质量为m=nM=36.5g/mol×15mol=547.5g,则所得盐酸溶液中溶质的质量分数为w=
=15mol,质量为m=nM=36.5g/mol×15mol=547.5g,则所得盐酸溶液中溶质的质量分数为w= ![]() ×100%≈35.4%,
×100%≈35.4%,
溶质的物质的量浓度为:c= ![]() mol/L≈10.5mol/L,
mol/L≈10.5mol/L,
所以答案是:(1)Ⅲ;分液漏斗;MnO2+4HCl(浓) ![]() MnCl2+Cl2↑+2H2O;(2)A;将湿润的淀粉KI试纸放在B口处,试纸变蓝色,证明氯气已集满;(3)NaOH溶液;2NaOH+Cl2=NaCl+NaClO+H2O;(4)10.5
MnCl2+Cl2↑+2H2O;(2)A;将湿润的淀粉KI试纸放在B口处,试纸变蓝色,证明氯气已集满;(3)NaOH溶液;2NaOH+Cl2=NaCl+NaClO+H2O;(4)10.5


 优等生题库系列答案
优等生题库系列答案科目:高中化学 来源: 题型:
【题目】同种物质中同一价态的元素部分被氧化,部分被还原的氧化还原反应是( )
A.3Br2+6KOH=5KBr+KBrO3+3H2O
B.MnO2+4HCl(浓) ![]() MnCl2+2H2O+Cl2↑
MnCl2+2H2O+Cl2↑
C.2KNO3 ![]() 2KNO2+O2↑
2KNO2+O2↑
D.NH4NO3 ![]() N2O↑+2H2O
N2O↑+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用98%的浓H2SO4(ρ=1.84g/cm3)配制500ml0.5mol/L的稀H2SO4 , 请按要求填空:
(1)所需浓H2SO4的体积为
(2)如果实验室有10mL、20mL、50mL量筒,应选用mL量筒,实验中用到的仪器除了烧杯、玻璃棒之外,还需要的仪器有:
(3)若实验中出现下列现象对所配溶液浓度有什么影响?(填偏高、偏低、无影响)
①浓硫酸溶解后未冷至室温即转移到容量瓶
②定容时俯视刻度线
③所用过的烧杯、玻璃棒未洗涤 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】核裂变产生的核能可以用于发电, ![]() U是一种常用的核燃料,下列说法错误的是( )
U是一种常用的核燃料,下列说法错误的是( )
A.![]() U相对原子质量为235
U相对原子质量为235
B.![]() U中的中子数为92
U中的中子数为92
C.![]() U与
U与 ![]() C的质量比约为235:12
C的质量比约为235:12
D.![]() U 与
U 与 ![]() U互称为同位素
U互称为同位素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】葡萄糖的结构简式为CH2OH—CHOH—CHOH—CHOH—CHOH—CHO,下列关于葡萄糖的说法错误的是( )
A. 葡萄糖是单糖B. 含有5个羟基(—OH)
C. 含有1个醛基(—CHO)D. 含有1个羧基(—COOH)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】全世界每年被腐蚀损耗的钢铁材料约占全年钢铁产量的十分之一.研究钢铁的腐蚀及防护有重要意义.回答下列问题:
(1)钢铁发生腐蚀的主要类型是电化学腐蚀,在电化学腐蚀中,负极反应是 , 正极反应是 .
(2)某实验小组设计图1实验探究铁生锈的条件: 
反应4min后观察,发现A处铁丝依然光亮,B处铁丝表面灰暗,D处铁丝依然光亮.该实验说明铁生锈主要与和有关;B、D处实验现象对比说明:决定铁生锈的一个重要因素是 .
(3)金属及塑料制品表面镀铬不仅美观还可提高金属制品抗腐蚀性能.常见镀铬液由重铬酸(H2Cr2O7)和催化剂硫酸组成.
①重铬酸中,Cr元素的化合价为 .
②镀铬时由CrO42﹣放电产生铬镀层.阴极的电极反应式为 .
(4)电镀废水中Cr2O72﹣具有高毒性,必须经处理后才能排放.电解法处理含铬的强酸性废水的原理如图2所示.
电解产生的Fe2+将Cr2O72﹣还原为Cr3+ , 再随着溶液pH的升高,便有Fe(OH)3和Cr(OH)3沉淀生成.
①图中A为电源极;电解时阴极产生的气体为(写化学式).
②写出Fe2+与Cr2O72﹣反应的离子方程式: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为制取纯净干燥的Cl2并让其与铁发生反应的装置,A是Cl2发生装置,C、D为气体净化装置,E硬质玻璃管中装有细铁丝网;F为干燥的空广口瓶;烧杯G为尾气吸收装置.试回答: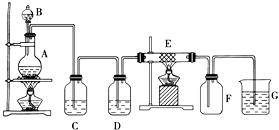
(1)C、G两个装置所盛放的试剂分别是:
CG .
(2)①装置搭好须进行气密性检查,写出操作方法: .
②两处酒精灯应先点燃处(填写A或B),目的是 .
③F中的现象为 , G中出现了一种沉淀,该沉淀的化学式 .
(3)写出在A、E中发生反应的化学方程式为:
A: .
E: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质的性质比较,正确的是( )
A. 酸性:H2SO4>HClO4>HBrO4 B. 碱性:NaOH>KOH>RbOH
C. 非金属性: P>S>Cl D. 气态氢化物稳定性:HF>H2O>PH3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com