
分析 (1)原子形成阳离子失去高能层中该能级电子,再失去同能层中低能级电子,然后再失去低能层中电子;
(2)Fe是26元素,其价电子数是8,每个配体CO分子提供电子数为2.
解答 解:(1)Fe原子核外电子排布为1s22s22p63s23p63d64s2,原子形成阳离子失去高能层中该能级电子,再失去同能层中低能级电子,然后再失去低能层中电子,故基态Fe3+的价电子排布式可表示为3d5,
故答案为:3d5;
(2)Fe是26元素,其价电子数是8,每个配体CO分子提供电子数为2,则8+2n=18,故n=5,故答案为:5.
点评 本题是对物质结构的考查,涉及核外电子排布、配合物,难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 做金属钠与水反应实验时,剩余的钠不能再放入原试剂瓶 | |
| B. | 酸式滴定管装标准液前,必须先用该溶液润洗 | |
| C. | 锥形瓶用作反应容器时一定不能加热 | |
| D. | 用容量瓶配溶液时,若加水超过刻度线,立即用滴定管吸出多余液体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaHC03水溶液显碱性,溶液中阳离子电荷总数小于阴离子电荷总数 | |
| B. | SiO2不跟碱反应,但可与氢氟酸反应 | |
| C. | NO2难液化,易溶于水并跟水反应 | |
| D. | Fe3O4能与浓盐酸反应生成FeCl2和FeCl3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C60、D2O、SiO2都属于化合物 | |
| B. | 漂白粉、石英、Fe(OH)3胶体都属于纯净物 | |
| C. | BaSO4、NH4Cl、NaOH都属于强电解质 | |
| D. | CO2、SO3、NO 都属于酸性氧化物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在稀硫酸中加入少量氢氧化钠固体,溶液导电性增强 | |
| B. | 饱和碳酸钠溶液中:c(Na+)=2c(CO32-) | |
| C. | 饱和食盐水中:c(Na+)+c(OH-)=c(Cl-)+c(H+) | |
| D. | pH=12的NaOH溶液中:c(OH-)=1.0×10-2 mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 容器中混合气体的平均相对分子质量增大 | |
| B. | 正反应速率增大,逆反应速率减小,平衡向正反应方向移动 | |
| C. | 正反应速率和逆反应速率都变小,C的百分含量增加 | |
| D. | 混合气体密度的变化情况不可以作为判断反应是否再次达平衡的依据 |
查看答案和解析>>
科目:高中化学 来源:2017届广东省高三月考二化学试卷(解析版) 题型:实验题
高铁酸钾广泛应用于净水、电池工业等领域。工业上以钛白粉生产的副产品FeSO4制备高铁酸钾的生产流程如下:

查资料得知K2FeO4的一些性质:
①在碱性环境中稳定,在中性和酸性条件下不稳定。
②在水中溶解度很大,难溶于无水乙醇等有机溶剂。
回答下列问题:
(1)写出氧化I中,生成Fe3+的离子反应方程式:
(2)氧化II中,试剂A为 (填“H2O2”或“HNO3”或“NaC1O”),反应的离子方程式为_____________________。
(3)操作I中包括冷却结晶,过滤洗涤、干燥几个步骤,洗涤干燥的目的是脱碱脱水,进行洗涤操作时应该用 洗涤。
(4)净水时高铁酸钾能逐渐与水反应生成絮状的Fe(OH)3,请补充并配平该反应方程式的系数及产物:
______K2FeO4 + H2O  Fe(OH)3(胶体)+ KOH + 。
Fe(OH)3(胶体)+ KOH + 。
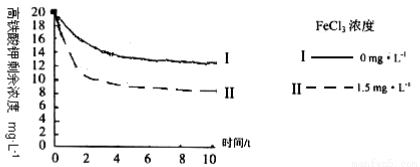
将一定量的K2FeO4投入一定浓度的FeC13溶液中,测得剩余K2FeO4浓度如下图所示,推测产生曲线I和曲线II差异的原因是: 。
(5)制得的粗K2FeO4产品中常混有少量KCl。取5.0 g粗产品溶于足量稀硝酸,充分反应后,加入足量的硝酸银,过滤得到沉淀,洗涤、干燥,称量得到1.435 g固体,K2FeO4的质量分数为___________。(可能用到的相对原子质量:O 16 Cl 35.5 K 39 Fe 56 Ag 108)
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 工业上制取Y的单质常用还原剂还原Y的氧化物 | |
| B. | Z的最高价氧化物能与水反应生成相应的酸 | |
| C. | 室温下,X的最高价氧化物的水溶液的pH>7 | |
| D. | Y单质在一定条件下可以与氧化铁发生置换反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 实验编号 | T/K | A的初始浓度/mol•L-1 | B的初始浓度/mol•L-1 | 催化剂的比表面积/m2•g-1 |
| Ⅰ | 200 | 0.40 | 0.60 | 82 |
| Ⅱ | T | 0.40 | 0.60 | 124 |
| Ⅲ | 220 | c1 | c2 | S |
| A. | T=200 | B. | S=100 | C. | c1=0.40 | D. | c2=0.60 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com