
| A. | SO3 | B. | NO2 | C. | Si | D. | CH3COOH |
分析 一定条件下,中学化学常见物质,甲、乙、丙、X之间存在“甲$\stackrel{x}{→}$乙$\stackrel{x}{→}$丙”的转化关系,依据选项中的各物质结合性质应用进行判断;
A、丙是三氧化硫,转化关系为,S$\stackrel{O_{2}}{→}$SO2$\stackrel{O_{2}}{→}$SO3;
B、丙为NO2,转化关系为:N2$\stackrel{O_{2}}{→}$NO$\stackrel{O_{2}}{→}$NO2;
C、丙若是硅,乙只能是二氧化硅和碳反应生成丙,甲到乙无法实现;
D、若丙为CH3COOH,则转化关系为:CH3CH2OH$\stackrel{O_{2}}{→}$CH3CHO$\stackrel{O_{2}}{→}$CH3COOH.
解答 解:一定条件下,中学化学常见物质,甲、乙、丙、X之间存在“甲$\stackrel{x}{→}$乙$\stackrel{x}{→}$丙”的转化关系,依据选项中的各物质结合性质应用进行判断;
A、若丙是三氧化硫,则可知甲可以为S,燃烧生成SO2,然后SO2在催化剂条件下与氧气生成SO3,转化关系为,S$\stackrel{O_{2}}{→}$SO2$\stackrel{O_{2}}{→}$SO3,故A正确;
B、若丙为NO2,则可知甲可以为N2,与氧气在放电调价下生成NO,然后NO在与氧气生成NO2,转化关系为:N2$\stackrel{O_{2}}{→}$NO$\stackrel{O_{2}}{→}$NO2,故B正确;
C、丙若是硅,乙只能是二氧化硅和碳反应生成丙,甲到乙无法实现,故C不能实现;
D、若丙为CH3COOH,则甲可以为CH3CH2OH,乙可以为CH3CHO,则转化关系为:CH3CH2OH$\stackrel{O_{2}}{→}$CH3CHO$\stackrel{O_{2}}{→}$CH3COOH,故D正确.
故选C.
点评 本题考查了元素化合物的性质应用,主要是两部反应的转化特征反应,熟练掌握物质性质是解题关键.


科目:高中化学 来源: 题型:选择题
| A. | 铁和稀硝酸反应:2Fe+6H+═2Fe3++3H2↑ | |
| B. | 铝与氢氧化钠溶液反应:Al+2OH-═AlO2-+H2↑ | |
| C. | 醋酸跟碳酸氢钠溶液反应:HCO3-+H+═CO2↑+H2O | |
| D. | 乙醇的催化氧化:2C2H5OH+O2→2CH3CHO+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
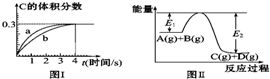
| A. | 该温度下,反应的平衡常数数值约为7.36 | |
| B. | 恒温条件下,缩小反应容器体积可以使反应的过程按图Ⅰ中a曲线进行 | |
| C. | 反应在第4秒钟达到化学平衡状态,0~4秒内,以A表示的化学反应速率是:0.225 mol•L-1•s-1 | |
| D. | 在上述反应体系中加入催化剂,化学反应速率增大,E1和E2均减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验组 | 温度/℃ | 起始量/mol | 平衡量/mol | 达到平衡所 需时间/min | ||
| H2O | CO | H2 | CO | |||
| 1 | 650 | 2 | 4 | 1.6 | 2.4 | 5 |
| 2 | 900 | 1 | 3 | 0.75 | 2.25 | 3 |
| 3 | 900 | 2 | 4 | x | y | t |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| CH4 | SiH4 | NH3 | PH3 | |
| 沸点(K) | 101.7 | 161.2 | 239.7 | 185.4 |
| 分解温度(K) | 873 | 773 | 1073 | 713.2 |
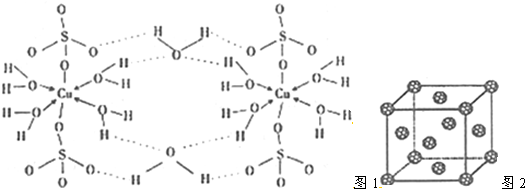
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 116号元素已被命名为“鉝”;2014年5月,科学家已确认发现117号元素,未命名,元素符号Uus;若将元素周期表的“一列”看作“一族”;则对117号元素的相关表述或性质推断错误的是( )
116号元素已被命名为“鉝”;2014年5月,科学家已确认发现117号元素,未命名,元素符号Uus;若将元素周期表的“一列”看作“一族”;则对117号元素的相关表述或性质推断错误的是( )| A. | 属第17族元素 | B. | 属非金属元素 | ||
| C. | 原子核外有117个电子 | D. | 有放射性 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
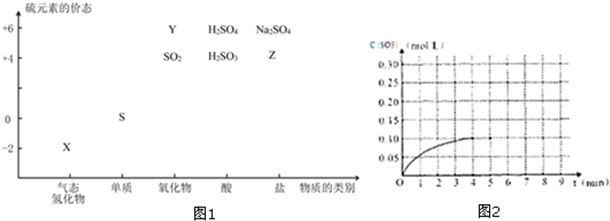
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C02分子中σ键和π键之比为1:1 | |
| B. | PCl5中所有原子均满足8电子稳定结构 | |
| C. | 由于HCOOH分子间存在氢键,则同压下,HC00H的沸点比CH3OCH3的高 | |
| D. | CH2=CH-CHO分子中碳原子的杂化类型均为sp2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com