
 两种有机物A、B的分子式均为C11H12O5,均能发生如图变化.
两种有机物A、B的分子式均为C11H12O5,均能发生如图变化.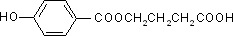 ,B为
,B为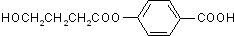 ,D为
,D为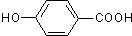 ,C发生缩聚反应生成高聚物E为
,C发生缩聚反应生成高聚物E为 ,F发生加聚反应生成高聚物I为
,F发生加聚反应生成高聚物I为 ,据此解答.
,据此解答.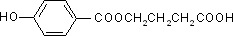 ,B为
,B为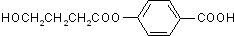 ,D为
,D为 ,C发生缩聚反应生成高聚物E为
,C发生缩聚反应生成高聚物E为 ,F发生加聚反应生成高聚物I为
,F发生加聚反应生成高聚物I为 ,
, ,含有的官能团为羧基和羟基,
,含有的官能团为羧基和羟基,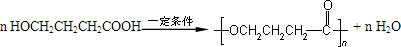 ,
, ;
;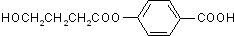 ,与足量氢氧化钠反应的方程式为
,与足量氢氧化钠反应的方程式为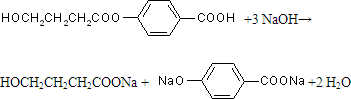 ,
, ;
; ,可以通过酯化反应进行的缩聚反应形成高聚物,故b正确;
,可以通过酯化反应进行的缩聚反应形成高聚物,故b正确;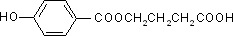 ,B为
,B为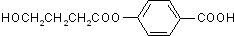 ,二者互为同分异构体,等质量的A与B,物质的量相等,每摩尔物质都消耗3molNaOH,故d正确;
,二者互为同分异构体,等质量的A与B,物质的量相等,每摩尔物质都消耗3molNaOH,故d正确; ,对应的同分异构体中符合:①苯环上的一卤代物有2种,说明苯环结构中只含有两种性质不同的氢原子,②与FeCl3溶液发生显色反应,说明含有酚羟基,③发生银镜反应,含有醛基或甲酸形成的酯,符合条件的有:
,对应的同分异构体中符合:①苯环上的一卤代物有2种,说明苯环结构中只含有两种性质不同的氢原子,②与FeCl3溶液发生显色反应,说明含有酚羟基,③发生银镜反应,含有醛基或甲酸形成的酯,符合条件的有: ,共有3种,
,共有3种,

 学习实践园地系列答案
学习实践园地系列答案科目:高中化学 来源: 题型:
| A、用8%的盐酸蒸发浓缩获得30%的盐酸 |
| B、光纤和餐桌上的瓷盘都是硅酸盐制品 |
| C、可利用丁达尔效应来区别淀粉溶液和氯化钠溶液 |
| D、二氧化硫具有漂白性,与氯水混合使用漂白效果更好 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
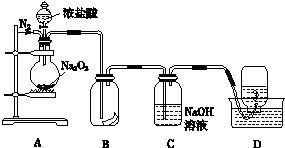
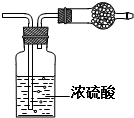 某无色气体可能由O2、CO、CO2、HCl、NH3、NO、Br2中的一种或几种组成,通过图中洗气瓶后气体体积减少(该装置前后都不与大气直接相连),通过干燥管(内盛放Na2O2)后气体呈红棕色,则下列推断正确的是( )
某无色气体可能由O2、CO、CO2、HCl、NH3、NO、Br2中的一种或几种组成,通过图中洗气瓶后气体体积减少(该装置前后都不与大气直接相连),通过干燥管(内盛放Na2O2)后气体呈红棕色,则下列推断正确的是( )| A、原气体中一定有NO和O2 |
| B、原气体中一定有NH3、NO、CO2、CO |
| C、原气体中一定没有CO |
| D、原气体中一定没有HCl、Br2、O2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
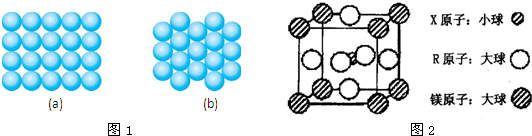
| X元素的基态原子中电子分布在三个不同的能级中,且每个能级中的电子总数相同 |
| Y元素的气态氢化物与其最高价氧化物对应的水化物能发生化合反应 |
| Z元素的族序数是其周期数的三倍 |
| W原子的第一至第六电离能分别为:I1=578KJ?mol-1 I2=1817KJ?mol-1 I3=2745KJ?mol-1I4=11575KJ?mol-1 I5=14830KJ?mol-1 I6=18376KJ?mol-1 |
| Q为前四周期中电负性最小的元素 |
| 元素R位于周期表的第10列 |
查看答案和解析>>
科目:高中化学 来源: 题型:
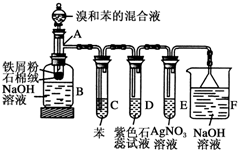 苯和溴取代反应的实验装置如图所示,其中A为由具支试管改制成的反应容器,在其下端开了一小孔,塞好石棉绒,再加入少量铁屑粉.填写下列空白:
苯和溴取代反应的实验装置如图所示,其中A为由具支试管改制成的反应容器,在其下端开了一小孔,塞好石棉绒,再加入少量铁屑粉.填写下列空白:查看答案和解析>>
科目:高中化学 来源: 题型:
 现有氨水、醋酸、盐酸、氯化铵四种溶液,请回答下列问题:
现有氨水、醋酸、盐酸、氯化铵四种溶液,请回答下列问题:| C(NH3?H2O) |
| C(OH-) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com