
下列叙述中不正确的是 ( )。
A.0.1 mol·L-1 NH4HS溶液中有:c(NH )<c(HS-)+c(S2-)+c(H2S)
)<c(HS-)+c(S2-)+c(H2S)
B.25 ℃时,将a mol·L-1的氨水与0.01 mol·L-1的盐酸等体积混合后,c(NH )=c(Cl-),则NH3·H2O的电离常数为
)=c(Cl-),则NH3·H2O的电离常数为
C.等浓度的HCN和NaCN混合溶液中有:2c(Na+)=c(CN-)+c(HCN)
D.等pH的①(NH4)2SO4溶液 ②NH4HSO4溶液 ③NH4Cl溶液中,c(NH )的大小关系:①>③>②
)的大小关系:①>③>②
解析 NH4HS溶液中存在NH 和HS-的水解平衡、HS-的电离平衡,由物料守恒知,c(NH
和HS-的水解平衡、HS-的电离平衡,由物料守恒知,c(NH )+c(NH3·H2O)=c(HS-)+c(S2-)+c(H2S),则c(NH
)+c(NH3·H2O)=c(HS-)+c(S2-)+c(H2S),则c(NH )<c(HS-)+c(S2-)+c(H2S),故A正确。氨水与盐酸反应后,c(NH
)<c(HS-)+c(S2-)+c(H2S),故A正确。氨水与盐酸反应后,c(NH )=c(Cl-)=0.005 mol·L-1,则c(H+)=c(OH-)=10-7 mol·L-1,溶液呈中性,Ka=
)=c(Cl-)=0.005 mol·L-1,则c(H+)=c(OH-)=10-7 mol·L-1,溶液呈中性,Ka= =
= ,B正确。HCN是弱酸,等浓度的HCN和NaCN混合溶液中根据物料守恒有2c(Na+)=c(CN-)+c(HCN),C正确。D中,pH相等时,①和③两溶液中c(NH
,B正确。HCN是弱酸,等浓度的HCN和NaCN混合溶液中根据物料守恒有2c(Na+)=c(CN-)+c(HCN),C正确。D中,pH相等时,①和③两溶液中c(NH )相同,NH
)相同,NH 的水解程度也相同;②NH
的水解程度也相同;②NH 的水解受到抑制,因此溶液中c(NH
的水解受到抑制,因此溶液中c(NH )最小,故D错误。
)最小,故D错误。
答案 D


科目:高中化学 来源: 题型:
下列说法正确的是 ( )
A.1 mL浓氨水加水稀释至l00mL后,溶液中n(OH-)减少
B.NaHCO3完全分解后的固体溶于水,所得溶液中不存在HCO3-
C.常温下,pH=3的醋酸和pH=11的NaOH溶液等体积混合后,溶液的pH<7
D.常温下,向NH4Cl溶液中加入氨水至溶液的pH=7,此时溶液中c(NH4+)>c(C1-)
查看答案和解析>>
科目:高中化学 来源: 题型:
与链烃相比,苯的化学性质的主要特征为( )
A.难氧化、难取代、难加成
B.易氧化、易取代、易加成
C.难氧化、易取代、难加成
D.易氧化、易取代、难加成
查看答案和解析>>
科目:高中化学 来源: 题型:
已知苯在一定条件下可发生烷基化取代反应:

①________________________________________________________________________,
②________________________________________________________________________,
③________________________________________________________________________,
④________________________________________________________________________,
⑤________________________________________________________________________,
⑥________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
根据下表提供的数据,判断在等浓度的NaClO、NaHCO3混合溶液中,各种粒子浓度关系正确的是 ( )。
| 化学式 | 电离常数 |
| HClO | Ka=3×10-8mol·L-1 |
| H2CO3 | Ka1=4.3×10-7mol·L-1 |
| Ka2=5.6×10-11mol·L-1 |
A.c(HCO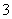 )>c(ClO-)>c(OH-)
)>c(ClO-)>c(OH-)
B.c(ClO-)>c(HCO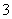 )>c(H+)
)>c(H+)
C.c(HClO)+c(ClO-)=c(HCO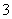 )+c(H2CO3)
)+c(H2CO3)
D.c(Na+)+c(H+)=c(HCO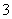 )+c(ClO-)+c(OH-)
)+c(ClO-)+c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
向等物质的量浓度的Na2S、NaOH混合溶液中滴加稀盐酸至过量。其中H2S、HS-、S2-的分布分数(平衡时某物质的浓度占各物质浓度之和的分数)与滴加盐酸体积的关系如图所示(忽略滴加过程中H2S气体的逸出)。
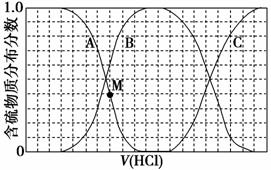
(1)B表示__________________。
(2)滴加稀盐酸至过量的过程中,溶液中微粒浓度的大小关系正确的是________(填字母)。
a.c(Na+)=c(H2S)+c(HS-)+2c(S2-)
b.2c(Na+)=c(H2S)+c(HS-)+c(S2-)
c.c(Na+)=3[c(H2S)+c(HS-)+c(S2-)]
(3)NaHS溶液呈碱性,当滴加盐酸至M点时,溶液中各离子浓度由大到小的顺序为:________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于合成氨工业的叙述可用勒夏特列原理来解释的是 ( )。
A.使用铁触媒,使平衡向生成NH3的方向移动
B.高压比常压条件更有利于合成氨的反应
C.500 ℃左右比室温更有利于合成氨的反应
D.合成氨时采用循环操作可提高原料的利用率
查看答案和解析>>
科目:高中化学 来源: 题型:
下列离子方程式正确的是
A.碳酸氢钠溶液与少量石灰水反应:HCO3-+Ca2++OH- =CaCO3↓+H2O
B.氯化铵与氢氧化钠两种浓溶液混合加热:NH4++OH-  H2O+NH3↑
H2O+NH3↑
C.氢氧化镁与稀硫酸反应:H+ +OH- =H2O
D.单质铜与稀硝酸反应:Cu+2H+ +2NO3-=Cu2+ +2NO↑+H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com