
【题目】酸性锌锰干电池和碱性锌锰干电池的构造简图如下所示,比较二者的异同,回答下列问题 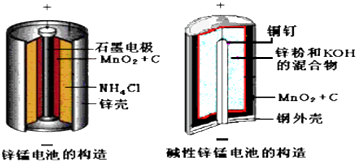
(1)酸性锌锰干电池的负极反应为 .
(2)碱性锌锰干电池在放电过程产生MnOOH,写出正极反应式 .
(3)维持电流强度为0.6A,电池工作10分钟,理论消耗Zng.(结果保留到小数点后两位,F=96500C/mol)
【答案】
(1)Zn﹣2e﹣=Zn2+
(2)MnO2+e﹣+H2O=MnOOH+OH﹣
(3)0.12
【解析】解:(1)酸性锌锰干电池的负极为锌,负极反应为Zn﹣2e﹣=Zn2+ , 所以答案是:Zn﹣2e﹣=Zn2+;(2)在碱性锌锰原电池中,Zn易失电子作负极、二氧化锰作正极,正极上二氧化锰得电子发生还原反应,电极反应式为MnO2+e﹣+H2O=MnOOH+OH﹣ , 所以答案是:MnO2+e﹣+H2O=MnOOH+OH﹣;(3)持电流强度为0.6A,电池工作10分钟,则电量为0.6A×600s=360C,转移电子的物质的量为 ![]() =0.00373mol则消耗Zn的质量为0.00373mol×
=0.00373mol则消耗Zn的质量为0.00373mol× ![]() ×65g/mol=0.12g,所以答案是:0.12.
×65g/mol=0.12g,所以答案是:0.12.


科目:高中化学 来源: 题型:
【题目】向四只盛有一定量NaOH溶液的烧杯中通入不同量的CO2气体后,在所得溶液中逐滴加入稀盐酸至过量,并将溶液加热,产生的CO2气体与HCl物质的量的关系如图(忽略CO2的溶解和HCl的挥发)。则下列分析都正确的组合是
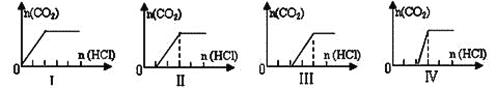
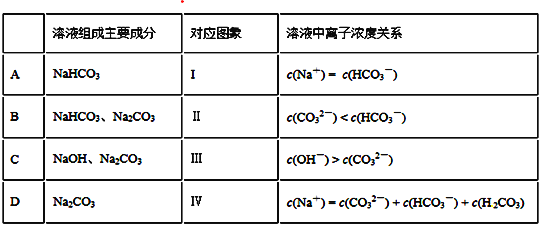
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列与金属腐蚀有关的说法正确的是( ) 
A.图a中,插入海水中的铁棒,越靠近底端腐蚀越严重
B.图b中,开关由M改置于N时,Cu﹣Zn合金的腐蚀速率减小
C.图c中,接通开关时Zn腐蚀速率增大,Zn上放出气体的速率也增大
D.图d中,Zn﹣MnO2干电池自放电腐蚀主要是由MnO2的氧化作用引起的
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于原电池和电解池的叙述正确的是( )
A.原电池中失去电子的电极为正极
B.电解时电解池的阳极一定是阴离子放电
C.原电池的两极一定是由活动性不同的两种金属组成的
D.原电池的负极、电解池的阳极都发生氧化反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用一种阴、阳离子双隔膜三室电解槽处理废水中的NH4+ , 模拟装置如图所示.下列说法正确的是( ) 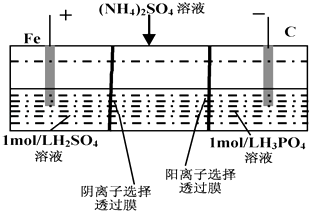
A.阳极室溶液由无色变成棕黄色
B.阴极的电极反应式为:4OH﹣﹣4e﹣=2H2O+O2↑
C.电解一段时间后,阴极室溶液中的酸性减弱
D.电解一段时间后,阴极室溶液中的溶质一定是(NH4)3PO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】温度一定时,于密闭容器中发生可逆反应:m A(g)+n B(g)![]() p C(g),达到平衡后,若将混合气体的体积压缩到原来的1/2,当再次达到平衡时,C的浓度为原平衡时C的浓度的1.9倍,则下列叙述中正确的是
p C(g),达到平衡后,若将混合气体的体积压缩到原来的1/2,当再次达到平衡时,C的浓度为原平衡时C的浓度的1.9倍,则下列叙述中正确的是
A. 平衡向逆反应方向移动 B. C气体的体积分数增大
C. 气体A的转化率升高 D. m+n>p
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把在空气中久置的铝片5.0 g投入盛有500 mL 0.5 mol·L-1硫酸溶液的烧杯中,该铝片与硫酸反应产生氢气的速率v与反应时间t可用如图坐标曲线来表示。下列推论错误的是( )

A. O~a段不产生氢气是因为表面的氧化物隔离了铝和硫酸溶液
B. b~c段产生氢气的速率增加较快的主要原因之一是温度升高
C. t>c时产生氢气的速率降低主要是因为溶液中c(H+)降低
D. t=c时反应处于平衡状态
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关物质性质与用途具有对应关系的是 ( )
A. Na2O2吸收CO2产生O2,可用作呼吸面具供氧剂
B. ClO2具有还原性,可用于自来水的杀菌消毒
C. Si晶体硬度大,可用于制造光导纤维
D. NH3易溶于水,可用作制冷剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】浓度均为0.10mol/L、体积均为V0的MOH和ROH溶液,分别加水稀释至体积V,pH随![]() 的变化如图所示,下列叙述错误的是( )
的变化如图所示,下列叙述错误的是( )

A. MOH的碱性强于ROH的碱性
B. ROH的电离程度:b点大于a点
C. 若两溶液无限稀释,则它们的c(OH-)相等
D. 当![]() =2时,若两溶液同时升高温度,则
=2时,若两溶液同时升高温度,则![]() 增大
增大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com