
【题目】室温下,用相同浓度的NaOH 溶液,分别滴定等体积且浓度均为0.1mol/L的三种酸(HA、HB 和HD)溶液,滴定的曲线如图所示,下列判断正确的是

A. 三种酸的电离常数关系:K(HD)>K(HB)>K(HA)
B. pH=7 时,三种溶液中:c(A-)=c(B-)=c(D-)
C. 当三种酸中和百分数达100%时,离子总浓度最大的是NaD 溶液
D. 滴定至P点时,溶液中:c(B-)>c(Na+)>c(HB)>c(H+)>c(OH-)
【答案】D
【解析】A. 相同物质的量浓度的一元酸,酸的pH越小,氢离子浓度越大,说明酸的电离程度越大,该酸的酸性越强,其电离平衡常数也越大,据图可知,未加NaOH溶液时,pH:HA<HB<HD,说明酸的电离程度HA>HB>HD,则K(HA)>K(HB)>K(HD),故A错误;B. 室温下,溶液的pH=7时,溶液中c(H+)=c(OH),根据电荷守恒,三种溶液中离子浓度关系为:c(Na+)+c(H+)=c(A)+c(OH),由c(H+)=c(OH)可知,c(Na+)=c(A),同理,c(Na+)=c(B)、c(Na+)=c(D),因A、B、D的水解程度不同,则溶液呈中性时消耗氢氧化钠溶液的体积不同,所得的三种溶液中钠离子浓度不同,所以c(A)、c(B)、c(D)也不同,故B错误;C. 当三种酸中和百分数达100%时,三种酸所消耗的氢氧化钠溶液体积相同,生成的钠盐浓度也相同,则三种溶液中c(Na+)相等,根据水解离子方程式可知,c(X)+c(OH)也相等(X代表A、B、D),因HD酸性最弱,D水解程度最大,则NaD溶液中c(OH)最大,c(H+)最小,所以c(Na+)+c(H+)+c(D)+c(OH)最小,故C错误 ;D. 滴定至P点时,HB溶液的中和百分数为50%,所得溶液中c(HB):c(NaB)=1:1,P点时溶液显酸性,说明HB的电离程度大于B的水解程度,c(H+)>c(OH),根据电荷守恒c(Na+)+c(H+)=c(OH)+c(B)可知,c(B)>c(Na+),因HB发生电离:HB![]() H++B,所以c(Na+)>c(HB)>c(H+),则c(B)>c(Na+)>c(HB)>c(H+)>c(OH),故D正确;答案选D。
H++B,所以c(Na+)>c(HB)>c(H+),则c(B)>c(Na+)>c(HB)>c(H+)>c(OH),故D正确;答案选D。


 计算高手系列答案
计算高手系列答案科目:高中化学 来源: 题型:
【题目】用铁片与稀硫酸反应制取氢气时,下列措施不能使反应速率加快的是( )
A.加热
B.不用稀硫酸改用98%的浓硫酸
C.滴加少量硫酸铜溶液
D.不用铁片,改用铁粉
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】英国曼彻斯特大学科学家安德烈·海姆和康斯坦丁。诺沃肖洛夫。共同工作多年的二人因“突破性地”用撕裂的方法成功获得超薄材料石墨烯而获诺贝尔奖。制备石墨烯方法有石墨剥离法、化学气相沉积法等。石墨烯的球棍模型示意图如下:

(1)下列有关石墨烯说法正确的是_________。
A.键长:石量烯>金刚石
B.石墨烯分子中所有原子可以处于同一平面
C.12g石墨烯含σ键数为NA
D.从石墨剥离得石墨烯需克服石墨层与层之间的分子间作用力
(2)化学气相沉积法是获得大量石墨烯的有效方法之一,催化剂为金、铜、钴等金属或合金,含碳源可以是甲烷、乙炔、苯、乙醇或酞菁等中的一种或任意组合。
①铜原子在基态时,在有电子填充的能级中,能量最高的能级符号为___________;第四周期元素中,最外层电子数与铜相同的元素还有_______________。
②乙醇的沸点要高于相对分子质量比它还高的丁烷,请解释原因_____________。
③下列分子属于非极性分子的是__________。
a.甲烷 b.二氯甲烷 c.苯 d.乙醇
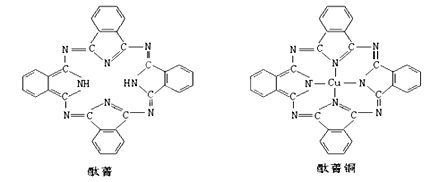
④酞菁与酞菁铜染料分子结构如图,酞菁分子中氮原子采用的杂化方式是__________;酞菁铜分子中心原子的配位数为____________。
⑤金与铜可形成的金属互化物合金(如图,该晶胞中,Au占据立方体的8个顶点),它的化学式可表示为____________;在Au周围最近并距离相等的Cu有___________个,若2个Cu原子核的最小距离为dpm,该晶体的密度可以表示为_________g/cm3。(阿伏伽德罗常数用NA表示)

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,对可逆反应3A(g) ![]() 2B(g) +C(g)的下列叙述中,能说明反应已达到平衡的是( )
2B(g) +C(g)的下列叙述中,能说明反应已达到平衡的是( )
A.C生成的速率与B分解的速率相等
B.单位时间内消耗3a mol A, 同时消耗生成a mol C
C.容器内的压强不再变化
D.混合气体的物质的量不再变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各项中的物质按电解质、非电解质、单质和混合物的顺序排列的一组是( )。
A.HCl、SO3、石墨、液氧B.蔗糖、CuSO4、氮气、CuSO4溶液
C.NaCl、乙醇、铁、空气D.KCl、NaNO3、氯气、石灰水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应A+3B==2C+4D(A、B、C、D均为气态),在四种不同情况下的反应速率最快的是
A. v(A)=0.1mol/(L·s) B. v(B) =0.6mol/(L·s)
C. v(C) =0.6mol/(L·s) D. v(D) =0.8mol/(L·s)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙醇可以发生下列化学反应,在反应里乙醇分子断裂碳氧键而失去羟基的是
A. 乙醇与金属钠反应 B. 乙醇与氢卤酸的取代反应
C. 乙醇的催化氧化反应 D. 乙醇和乙酸的酯化反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在照相底片的定影过程中,未曝光的溴化银(AgBr)常用硫代硫酸钠(Na2S2O3)溶解,反应生成Na3[Ag(S2O3)2];在废定影液中加人Na2S使Na3[Ag(S2O3)2]中的银转化为Ag2S,并使定影液再生。将Ag2S在高温下转化为Ag,就达到了回收银的目的。
(1)铜、银、金在元素周期表中位于同一族相邻周期,基态银原子的最外层电子排布式为 _______。
(2)Na、O、S简单离子半径由大到小的顺序为______________________。
(3)S2O32-离子结构如图所示,其中心硫原子的杂化轨道类型为_______________________。

(4)写出AgBr 溶于Na2S2O3溶液的离子反应方程式______________。Na3[Ag(S2O3)2]中存在的作用力有离子键、共价键、______________。
(5)在空气中灼烧Ag2S生成Ag和SO2,SO2 分子中硫原子的价层电子对数为_________,其分子空间构型为______________。 SO2易溶于水,原因是________________________________。
(6)现在人们已经有多种方法来测定阿伏加德罗常数,X射线衍射法就是其中的一种,通过对金晶体的X 射线衍射图象的分析,可以得出金晶体的晶胞属于面心立方晶胞(与铜的晶胞相似)。若金原子的半径为am,金的密度为ρg·cm-3,金的摩尔质量为Mg·mol -1,试通过这些数据列出计算阿伏加德罗常数的算式______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列水解化学方程式或水解离子方程式正确的是: ( )
A.CH3COO- + H2O ![]() CH3COOH + OH-
CH3COOH + OH-
B.NH4+ + H2O=NH4OH + H+
C.CH3COOH + NaOH ![]() CH3COONa + H2O
CH3COONa + H2O
D.NaCl + H2O ![]() NaOH + HCl
NaOH + HCl
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com