
 暑假作业海燕出版社系列答案
暑假作业海燕出版社系列答案 本土教辅赢在暑假高效假期总复习云南科技出版社系列答案
本土教辅赢在暑假高效假期总复习云南科技出版社系列答案 暑假作业北京艺术与科学电子出版社系列答案
暑假作业北京艺术与科学电子出版社系列答案科目:高中化学 来源: 题型:
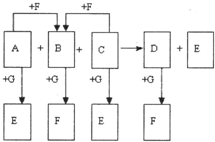 (2010?金华模拟)已知图中所有物质均为化合物,A、C的水溶液呈碱性,且C是一种强碱,F、G的水溶液呈酸性.B为红褐色沉淀,化合物G在常温下呈气态,其水溶液是一种常见的强酸,A、C、D、E焰色反应呈黄色.A、D的水溶液都有杀菌消毒作用. A、B、C反应时,物质的量之比为3:2:4.其它物质相互间的转化关系如图所示(各反应在常温下即可发生;多数反应的生成物没有写完整).请写出:
(2010?金华模拟)已知图中所有物质均为化合物,A、C的水溶液呈碱性,且C是一种强碱,F、G的水溶液呈酸性.B为红褐色沉淀,化合物G在常温下呈气态,其水溶液是一种常见的强酸,A、C、D、E焰色反应呈黄色.A、D的水溶液都有杀菌消毒作用. A、B、C反应时,物质的量之比为3:2:4.其它物质相互间的转化关系如图所示(各反应在常温下即可发生;多数反应的生成物没有写完整).请写出: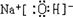
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
 (2010?揭阳模拟)草酸(H2C2O4)是一种有机二元酸,水溶液中草酸的存在形态有三种,各形态的浓度分数α(H2C2O4-α0,HC2O4--α1,C2O42--α2)随溶液pH变化的关系如图所示.
(2010?揭阳模拟)草酸(H2C2O4)是一种有机二元酸,水溶液中草酸的存在形态有三种,各形态的浓度分数α(H2C2O4-α0,HC2O4--α1,C2O42--α2)随溶液pH变化的关系如图所示.| c(Na+) | ||
c(
|
| c(Na+) | ||
c(
|
| ||
| ||
| 酸 | 铁锈[Fe(OH)3]溶解量/g | 水垢(CaCO3)溶解量/g |
| 盐酸 | 0.7911 | 全溶 |
| 磷酸 | 0.1586 | 微溶 |
| 草酸 | 0.7399 | 0.0036 |
| 醋酸 | 0.1788 | 0.1655 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||

查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
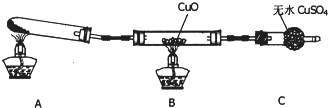
| H+ |
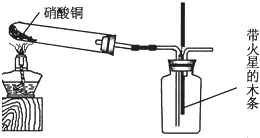
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
 火柴头中硫元素、氯元素的检验
火柴头中硫元素、氯元素的检验
【实验情景】
实验一:取两只洁净的小烧杯,标记为甲、乙,在乙烧杯中加入10ml 0.01mol?L-1KMnO4酸性溶液。将两根火柴伸入甲烧杯里,再用一根燃着的火柴点燃火柴头(如右图所示),待火柴头燃尽,即将火柴移出,迅速将甲烧杯倒扣在乙烧杯上,轻轻振荡乙烧杯,观察实验现象。
实验二:用漏斗、试管、注射器、导管等组成如右图装置,将两 根火柴放在漏斗下面,用一根燃着的火柴点燃火柴头,使火柴头燃烧。慢慢拉动注射器的活塞进行抽气,让火柴头燃烧产生的气体通过 0.01mol?L-1KMnO4酸性溶液,观察实验现象。
0.01mol?L-1KMnO4酸性溶液,观察实验现象。
实验三:将燃尽的火柴头浸泡在少量水中,片刻后取少量溶液于 试管中,滴加AgNO3和稀硝酸,观察实验现象。
实验四:将3-4根火柴头摘下浸于水中,片刻后取少量溶液于试管中,加AgNO3溶液、稀硝酸和NaNO2溶液,观察实验现象。
【问题设计】
问题1:安全火柴盒侧面涂有红磷(发火剂)和Sb2O3(易燃物)等,火柴头上的物质一般是 、 等氧化剂和 等易燃物。
问题2:实验一和实验二均可观察到的实验现象是 ,请用化学方程式说明产生这种现象的原因 。
实验一设计的方案还利用了SO2的一种 性质。
问题3:写出以下反应的化学方程式:
(1) 将SO2通入氯水中,浅黄绿色褪成无色
体现了SO2的 性。
(2) 将SO2通入溴水中,红棕色褪为无色
体现了SO2的 性。
(3) 将SO2通入无色的氢硫酸溶液,溶液变浑浊
体现了SO2的 性。
问题4:实验三可观察到白色沉淀 产生,说明将燃尽的火柴头浸泡在少量水中,会有 物质被浸出,产生该物质的反应方程式为 ,
主要是把火柴头中含有的 转化为 。
问题5:实验四产生的白色沉淀为 ,NaNO2的作用是 ,
反应的离子方程式为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com