
莽草酸因可以作为合成达菲(抗病毒和抗癌药)的中间体而受到重视,其结构简式如图,下列关于莽草酸的说法正确的是
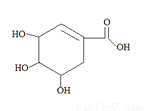
A.分子中含有三种含氧官能团
B.可发生取代、加成及氧化反应
C.在水溶液中羟基和羧基均能电离出氢离子
D.与足量的钠反应能产生44.8L气体
科目:高中化学 来源:2016届江苏省高三5月四模化学试卷(解析版) 题型:选择题
常温下,下列各组离子在指定溶液中一定能大量共存的是
A.能溶解A12O3的溶液:Na+, K+, HCO3一 , NO3-
B.0.lmol/LCa(C1O)2溶液:K+, Na+, I一、Cl-
C.能使甲基橙显红色的溶液:K+, Fe2+, Cl-, NO3-
D.加入KSCN显红色的溶液:Na+, Mg 2+, Cl-, SO42-
查看答案和解析>>
科目:高中化学 来源:2015-2016学年内蒙古杭锦后旗奋斗中学高二下期中化学卷(解析版) 题型:选择题
用pH均为2的盐酸和醋酸溶液,分别中和等体积、等物质的量浓度的氢氧化钠溶液,当氢氧化钠恰好完全中和时,消耗盐酸和醋酸溶液的体积分别为V1和V2,则V1和V2的关系正确的是( )
A. V1>V2 B. V1<V2 C. V1=V2 D. V1≤V2
查看答案和解析>>
科目:高中化学 来源:2015-2016学年内蒙古杭锦后旗奋斗中学高二下期中化学卷(解析版) 题型:选择题
某一反应物的浓度是1.0 mol·L-1,经过20 s后,它的浓度变成了0.2 mol·L-1,在这20 s内用该物质浓度变化表示的化学反应速率为( )
A.0.04 B.0.04 mol·L-1·s-1
C.0.08 mol·L-1·s-1 D.0.04 mol·L-1
查看答案和解析>>
科目:高中化学 来源:2016届山西省等校高三下第四次联考理综化学A卷(解析版) 题型:选择题
常温下,将一元酸HA和NaOH溶液等体积混合,两种溶液的浓度和混合后所得溶液的pH如下表:
实验编号 | c(HA)/mol·L-1 | c(NaOH)/mol·L-1 | 混合溶液的pH |
甲 | 0.1 | 0.1 | pH=a |
乙 | 0.2 | 0.2 | pH=9 |
丙 | c1 | 0.2 | pH =7 |
丁 | 0.2 | 0.1 | pH<7 |
下列判断正确的是
A.c1=0.2 B.丁组混合液:c(Na+)>c(A-)>c(H+)>c(OH-)
C.a>9 D.在乙组混合液中由水电离出的c(OH-)=10-5mol·L-1
查看答案和解析>>
科目:高中化学 来源:2016届黑龙江省高三考前训练二理综化学试卷(解析版) 题型:填空题
二氯化砜(SO2Cl2)是一种无色液体,主要用于有机物和无机物的氯化等。其熔点为-54.1℃.沸点为69.2℃;常温下比较稳定,受热易分解,遇水剧烈反应生成硫酸和盐酸。
(1)制备。实验室可利用SO2和Cl2按下列装置制取少量SO2Cl2(丙中放有樟脑液,起催化作用)。已知SO2(g)+Cl2(g) SO2Cl2(g) △H<0
SO2Cl2(g) △H<0

①可以用浓盐酸和酸性高锰酸钾制取氯气,该反应的化学方程式为 ;溶液A为 。
②上图实框中仪器己的名称为 ;反应装置图的虚框中未画出的仪器是 (填“己”或“庚”)。
③如果将丙装置放入冰水中,会更有利于二氯化砜的生成,其原因是 。
④下列有关说法错误的是 (填编号)。
a.乙、戊装置相同,在实验中的作用也完全相同
b.甲、丁装置为洗气装置,可用于气体的除杂和干燥
c.组装仪器后首先要进行的操作是检查装置的气密性
d.为提高反应物的利用率,可控制甲、丁装置中产生气泡的速率相等
(2)提纯。将收集到的产物进行减压蒸馏,减压蒸馏的目的是 。
(3)测定。取1.00g蒸馏后液体,小心地完全溶于水,向所得的溶液中加入足量氯化钡溶液,测得生成沉淀的质量为1.60g,则所得蒸馏成分中二氯化砜的质量百分含量为 %。
(4)贮存。二氯化砜应储存于阴凉、干燥、通风良好的库房。但久置后微显黄色,其原因是 。
查看答案和解析>>
科目:高中化学 来源:2016届黑龙江省高三考前训练二理综化学试卷(解析版) 题型:选择题
下列有关说法不正确的是( )
A.沿海城市建筑时直接从海洋里取用海沙,可以大大降低成本
B.“地沟油”禁止使用,但处理后可以制生物柴油和肥皂
C.乙醇溶液、双氧水均可用于杀菌消毒,但原理不同
D.维生素C和铁粉是常用的抗氧化剂
查看答案和解析>>
科目:高中化学 来源:2015-2016学年新疆兵团农二师华山中学高一下期中化学卷(解析版) 题型:选择题
漂白粉的有效成分是( )
A.Ca(OH)2 B.Ca(ClO)2 C.CaCl2 D.CaCO3
查看答案和解析>>
科目:高中化学 来源:2015-2016学年吉林省高一下期中化学试卷(解析版) 题型:选择题
随着碱金属、卤素原子半径的增大,下列递变规律正确的是
A.碱金属和卤素单质的熔沸点都逐渐降低
B.碱金属和卤素单质的密度都依次变大
C.卤素的气态氢化物稳定性逐渐增强
D.碱金属单质还原性逐渐增强
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com