
| A. | Mg2+、SO42-、K+、Cl- | B. | Na+、NH4+、NO3-、Fe3+ | ||
| C. | K+、CO32-、Cl-、Br- | D. | Ba2+、Na+、OH-、SO42- |
 全程金卷系列答案
全程金卷系列答案 快乐5加2金卷系列答案
快乐5加2金卷系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,48g O3含有的分子数为NA | |
| B. | 1molNa2O2晶体中阴离子数为2 NA | |
| C. | 标准状况下,33.6L的 四氯化碳(CCl4)中含有的碳原子数目为1.5NA | |
| D. | 常温常压下,7.1 g Cl2与足量的Fe充分反应,转移的电子数目为0.3 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Fe2(SO4)3 | B. | KNO3 | C. | Na2SO4 | D. | FeSO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
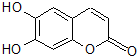 中草药秦皮中含有的七叶树内酯(如图)具有抗菌作用.若1mol该物质分别与浓溴水和H2完全反应,则消耗的Br2和H2的物质的量最多分别为( )
中草药秦皮中含有的七叶树内酯(如图)具有抗菌作用.若1mol该物质分别与浓溴水和H2完全反应,则消耗的Br2和H2的物质的量最多分别为( )| A. | 2molBr2 3molH2 | B. | 2molBr2 4molH2 | C. | 3molBr2 4molH2 | D. | 3molBr2 5molH2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径由小到大排序为:X<Y<Z<W | |
| B. | Z的最高价氧化物既能与某酸反应,又能与某碱反应,属于两性物质 | |
| C. | Y单质在一定条件下可以跟四氧化三铁发生置换反应 | |
| D. | 室温下,0.1 mol•L-1 W的气态氢化物的水溶液中氢离子的浓度为0.2mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com