
可逆反应aA(g)+bB(g)
 cC(g)的正、逆反应速率可用各反应物或生成物浓度的变化来表示。下列各关系式中能说明反应已达到平衡状态的是( )
cC(g)的正、逆反应速率可用各反应物或生成物浓度的变化来表示。下列各关系式中能说明反应已达到平衡状态的是( )
A.av正(A)=bv正(B) B.bv正(A)=av逆(B)
C.av正(C)=cv正(A) D.av正(A)=bv逆(B)
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
SiCl4在室温下为无色液体,易挥发,有强烈的刺激性。把SiCl4先转化为SiHCl3,再经氢气还原生成高纯硅。一定条件下,在20L恒容密闭容器中发生SiCl4转化为SiHCl3 的反应:3SiCl4(g)+2H2(g)+Si(s) 4SiHCl3(g) ΔH=Q kJ·mol-1。2 min后达到平衡,H2与SiHCl3的物质的量浓度分别为0.1 mol·L-1和0.2 mol·L-1。
4SiHCl3(g) ΔH=Q kJ·mol-1。2 min后达到平衡,H2与SiHCl3的物质的量浓度分别为0.1 mol·L-1和0.2 mol·L-1。
(1)从反应开始到平衡,v(SiCl4)= 。
(2)该反应的平衡常数表达式为K= ,温度升高,K值增大,则Q 0(填“>”、“<”或“=”)。
 (3)若平衡后再向容器中充入与起始时等量的SiCl4和H2(假设Si足量),当反应再次达到平衡时,与原平衡相比较,H2的体积分数将 (填“增大”、“减小”或“不变”)。
(3)若平衡后再向容器中充入与起始时等量的SiCl4和H2(假设Si足量),当反应再次达到平衡时,与原平衡相比较,H2的体积分数将 (填“增大”、“减小”或“不变”)。
(4)原容器中,通入H2的体积(标准状况下)为 。
(5)平衡后,将容器的体积缩为10 L,再次达到平衡时,
H2的物质的量浓度范围为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知难溶电解质在水溶液中存在溶解平衡:
MmAn(s)
 mMn+(aq)+nAm-(aq)
mMn+(aq)+nAm-(aq)
Ksp=[Mn+]m·[Am-]n,称为溶度积。
某学习小组欲探究CaSO4沉淀转化为CaCO3沉淀的可能性,查得如下资料:(25℃)
| 难溶电 解质 | CaCO3 | CaSO4 | MgCO3 | Mg(OH)2 |
| Ksp | 2.8×10-9 mol-2·L-2 | 9.1×10-6 mol-2·L-2 | 6.8×10-6 mol-2·L-2 | 1.8×10-12 mol-3·L-3 |
实验步骤如下:
①往100 mL 0.1 mol·L-1的CaCl2溶液中加入100 mL 0.1 mol·L-1的Na2SO4溶液,立即有白色沉淀生成。
②向上述悬浊液中加入固体Na2CO3 3 g,搅拌,静置,沉淀后弃去上层清液。
③再加入蒸馏水搅拌,静置,沉淀后再弃去上层清液。
④________________________________________________________________________。
(1)由题中信息知Ksp越大,表示电解质的溶解度越______(填“大”或“小”)。
(2)写出第②步发生反应的化学方程式:
________________________________________________________________________
________________________________________________________________________。
(3)设计第③步的目的是
________________________________________________________________________。
(4)请补充第④步操作及发生的现象:
________________________________________________________________________
________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
在基态多电子原子中,关于核外电子能量的叙述错误的是 ( )。
A.最易失去的电子能量最高
B.电离能最小的电子能量最高
C.p轨道电子能量一定高于s轨道电子能量
D.在离核最近区域内运动的电子能量最低
查看答案和解析>>
科目:高中化学 来源: 题型:
物质结构决定性质,深入研究物质的微观结构,有利于理解物质变化的本质。请回答下列问题:
(1)C、Si、N的电负性由大到小的顺序是________;C、N、O、F的第一电离能由大到小的顺序是________。
(2)A、B均为短周期金属元素。依据表中的数据,写出B原子的电子排布式:________。
| 电离能/(kJ·mol-1) | I1 | I2 | I3 | I4 |
| A | 932 | 1 821 | 15 390 | 21 771 |
| B | 738 | 1 451 | 7 733 | 10 540 |
(3)过渡金属离子与水分子形成的配合物是否有颜色,与其d轨道电子排布有关。一般而言,为d0或d10排布时,无颜色;为d1~d9排布时,有颜色,如[Co(H2O)6]2+显粉红色。据此判断,[Mn(H2O)6]2+________颜色(填“无”或“有”)。
(4)L的原子核外电子占有9个轨道,而且有一个未成对电子,L是________(填元素符号)。
查看答案和解析>>
科目:高中化学 来源: 题型:
锑(Sb)在自然界一般以硫化物的形式存在。从硫化物中提取单质锑一般是先在高温下将硫化物转化为氧化物,再用碳还原:
2Sb2S3+3O2+6Fe===Sb4O6+6FeS ①
Sb4O6+6C===4Sb+6CO ②
关于反应①、反应②的说法正确的是 ( )。
A.反应①②中的氧化剂分别是Sb2S3、Sb4O6
B.反应①中每生成3 mol FeS时,共转移6 mol电子
C.反应②说明高温下Sb的还原性比C强
D.每生成1 mol Sb时,反应①与反应②中氧化剂的物质的量之比为1∶3
查看答案和解析>>
科目:高中化学 来源: 题型:
下列离子方程式中,正确的是 ( )
A.向Mg(HCO3)2溶液中加入过量的NaOH溶液
Mg2++2HCO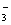 +2OH—
+2OH— MgCO3↓+ CO32-+2H2O
B.溴化亚铁溶液中通入足量的氯气:2Fe2++Cl2=2Fe3++2Cl-
C.少量的CO2通入稀的碳酸钠溶液中:CO2+CO32-+H2O 2HCO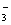
D.向NH4Al(SO4)2溶液中滴入Ba(OH)2使SO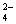 反应完全
反应完全
2Ba2++4OH—+Al3++2SO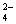
2BaSO4↓+AlO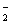 +2H2O
+2H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com