
【题目】镁、铝、铜三种金属粉末混合物,加入过量盐酸充分反应,过滤后向滤液中加入过量烧碱溶液,再过滤,滤液中存在的离子有( )
A.Al3+ B.Cu2+ C.AlO2- D.Mg2+
 黄冈小状元同步计算天天练系列答案
黄冈小状元同步计算天天练系列答案科目:高中化学 来源: 题型:
【题目】2016年夏季奥运会将在“足球王国”﹣﹣巴西首都里约热内卢举行,如图酷似奥林匹克旗中的五环的一种有机物被称之为奥林匹克烃,下列说法正确的是( )
![]()
A. 该有机物属于芳香族化合物,是苯的同系物
B. 该有机物中只含非极性键
C. 该有机物的一氯代物有11种
D. 该有机物完全燃烧生成H2O的物质的量小于CO2的物质的量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下面用序号给出了周期表中的部分元素,请从①~⑧中选择合适的元素回答下列问题:
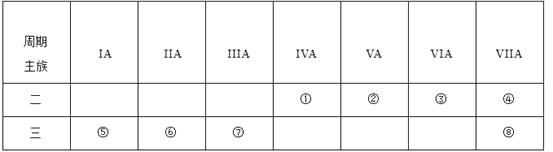
(1)上述元素中原子半径最大的是(填元素符号) ,气态氢化物最稳定的是(填化学式,下同) ,气态氢化物水溶液呈碱性的是 ,最高价氧化物对应水化物酸性最强的是 .
(2)元素①与③按原子个数1:2构成的分子的电子式为 .
(3)元素⑤和⑦的最高价氧化物对应水化物反应的离子方程式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(10分) “酒是陈的香”,就是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室我们也可以用如图所示的装置制取乙酸乙酯.回答下列问题:

(1)写出制取乙酸乙酯的化学反应方程式 .
(2)浓硫酸的作用是:① ② .
(3)饱和碳酸钠溶液的主要作用是 .
(4)装置中通蒸气的导管要插在饱和碳酸钠溶液的液面上,不能插入溶液中,目的是防止 .
(5)若要把制得的乙酸乙酯分离出来,应采用的实验操作是 .
(6)做此实验时,有时还向盛乙酸和乙醇的试管里加入几块碎瓷片,其目的是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I:中学实验进行电解饱和食盐水时可从下图中选用必要的装置,并要求测定产生氢气的体积(大于25 mL),和检验氯气的氧化性。
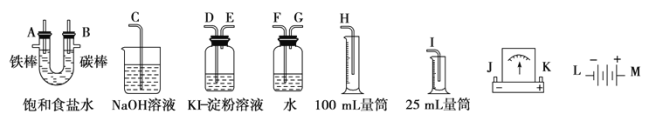 (1)写出电解饱和食盐水的离子方程式______________。
(1)写出电解饱和食盐水的离子方程式______________。
(2)电源、电流表与A、“两极的正确连接顺序为:L→( )→( )→( )→( )→M。
(3)该实验测定产生氢气的体积时,选用的量筒为__________(填25 mL量筒或50 mL量筒)
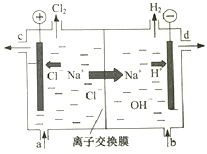
II:工业中的氯碱工业是离子交换膜法电解精制饱和食盐水如下图,离子交换膜只允许阳离子通过。
完成下列填空:
(4)粗食盐的水溶液含有SO42-、Ca2+、Mg2+。若要除去SO42-,则需加的试列为___________。
(5)精制饱和食盐水从图中_位置补充,氢氧化钠溶液从图中________位置流出(选填“a”、“”“b”、“c”或“d”)
(6)0.1mol/L的Na2SO3溶液中各离子浓度从人到小的顺序为___________。
(7)室温下,0.1mol/L的NaClO溶液的pH________0.1mol/L的Na2SO3溶液的pH.(选填“大于”、“小于”或“等于”)(已知:H2SO3 K1=1.54×10-2 K2=1.02×10-7 ;HClO K=2.95×10-8)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)某学生为了探究锌与盐酸反应过程中的速率变化,他在100mL稀盐酸中加入足量的锌粉,用排水集气法收集反应放出的氢气(标准状况下),实验记录如下(累计值):
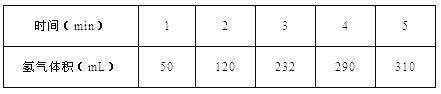
① 哪一时间段(指0~1、1~2、2~3、3~4、4~5min)反应速率最大_______。
②2~3分钟时间段以盐酸的浓度变化来表示的该反应速率______。(设溶液体积不变)
③如果反应太激烈,为了减缓反应速率而又不减少产生氢气的量,他在盐酸中分别加入等体积的下列溶液:
A.蒸馏水、B.NaCl溶液、C.NaNO3溶液 D.CuSO4溶液 E.Na2CO3溶液,你认为可行的是___________。
(2)将等物质的量A、B混合于2L密闭容器中,发生如下反应3A(g)+B(g) ![]() xC(g)+2D(g),经5分钟后,测得D的浓度为0.5mol/L,此时A的浓度与B的浓度之比为3:5,C的平均反应速率是0.1mol/(L·min) 则平衡时A的浓度为__________mol/L,B的平均反应速率 ______mol/(L·min)。
xC(g)+2D(g),经5分钟后,测得D的浓度为0.5mol/L,此时A的浓度与B的浓度之比为3:5,C的平均反应速率是0.1mol/(L·min) 则平衡时A的浓度为__________mol/L,B的平均反应速率 ______mol/(L·min)。
(3)已知断裂1molC-H,O=O,C=O,H-O化学键所需能量分别为akJ,bkJ,ckJ,dkJ,则该反应CH4+O2=CO2+2H2O的反应热为△H=________kJ/mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是( )
A.漂白粉在溶液中存在平衡:ClO-+H2O![]() HClO+OH-,加少量NaOH能提高其漂白效率
HClO+OH-,加少量NaOH能提高其漂白效率
B、硫酸钡难溶子水,但硫酸钡属于强电解质
C、滴定前滴定管内无气泡,终点读数时有气泡,所测体积偏大
D、物质的量浓度相同的四种溶液:①氯化铵②硫酸氢铵 ③次氯酸铵④碳酸铵的pH:④>②>①>③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作正确的是( )
A.蒸馏时,将温度计的水银球插入液面下
B.称量时,将硫酸铜晶体直接放在天平右盘上称量
C.加热时,将烧杯、试管直接放在酒精灯上加热
D.闻气味时,将少量的气体用手轻轻扇入鼻孔中
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一定量的SO2和O2充入一个容积固定的密闭容器中,在一定条件下发生反应:2SO2(g)+O2(g)![]() 2SO3(g),下列哪个量不再变化时,并不能说明化学反应已达到平衡状态
2SO3(g),下列哪个量不再变化时,并不能说明化学反应已达到平衡状态
A.混合气体的密度
B.混合气体的压强
C.混合气体的平均摩尔质量
D.SO2的转化率
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com