
 �ֱ�����йط�Ӧ�е�һ�����ʣ�����д���¿հף�
�ֱ�����йط�Ӧ�е�һ�����ʣ�����д���¿հף�
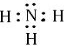 ��
��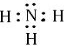 ��
��
| ||
| �� |
| ||
| �� |
| ||
| ||
| 5 |
| 4 |
| 6 |
| 5 |
| 4 |
| 5 |
| 2 |
| 3 |
| 23 |
| 12 |
| 1 |
| 12 |


 ȫ�ŵ�����Ԫ�ƻ�ϵ�д�
ȫ�ŵ�����Ԫ�ƻ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����pH��ֽ�ⶨ���Ƚ�Ũ�Ⱦ�Ϊ0.1 mol/L������ʹ����pH |
| B����0.1 mol/L NaOH��Һ�ֱ��к͵������Ũ�ȵ�����ʹ��ᣬ�Ƚ�����NaOH��Һ����� |
| C����ȡ1mL����ʹ�����Һ���ֱ����pH��pH��Ϊ1����ˮ��ϡ�͵�1000�����Ƚ�ϡ�ͺ���Һ��pH |
| D����pH��ֽ�ⶨ���Ƚϵ�Ũ�ȵ��Ȼ��ƺʹ���������Һ��pH |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
A��b��40y��2-
| ||
B��b��80y��2-
| ||
C��b��40y��1-
| ||
D��b��80y��1-
|
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����Ƭ��ϡ����ķ�Ӧ |
| B��þ��ȼ�� |
| C�����ȵ�̼��CO2�ķ�Ӧ |
| D����������ˮ��Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ijС��������ϵ�֪��C2O42-+MnO4-+H+��CO2��+Mn2++H2O��δ��ƽ���������ø÷�Ӧ�ⶨij�����ƣ�Na2C2O4����Ʒ�в����Ƶ�������������С�����1.34g��������Ʒ����ϡ�����У�Ȼ����0.200mol?L-1�����Ը��������Һ���еζ������е����ʲ���������غ�ϡ���ᷴӦ����
ijС��������ϵ�֪��C2O42-+MnO4-+H+��CO2��+Mn2++H2O��δ��ƽ���������ø÷�Ӧ�ⶨij�����ƣ�Na2C2O4����Ʒ�в����Ƶ�������������С�����1.34g��������Ʒ����ϡ�����У�Ȼ����0.200mol?L-1�����Ը��������Һ���еζ������е����ʲ���������غ�ϡ���ᷴӦ�����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

| A��1 mol N2��g����1 mol O2��g����Ӧ�ų�������Ϊ180 kJ |
| B��1 mol N2��g����1 mol O2��g�������������2 mol NO��g����������� |
| C��ͨ������£�N2��g���� O2�����ֱ������NO |
| D��NO��һ���������������NaOH��Һ��Ӧ�����κ�ˮ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ||
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����ȼ |
| B������KMnO4��Һ |
| C��ͨ����ˮ |
| D��ͨ��Cl2����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��1 mol/L |
| B��2 mol/L |
| C��0.5 mol/L |
| D��0.2 mol/L |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com