
下列实验设计及其对应的离子方程式均正确的是
A.用FeCl3溶液腐蚀铜箔制作印刷电路板:Fe3++Cu===Cu2++Fe2+
B.用Na2CO3溶液处理水垢中的CaSO4:CO32-+CaSO4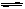 CaCO3+SO42-
CaCO3+SO42-
C.碳酸钠溶液显碱性:CO32-+2H2O H2CO3+2OH-
H2CO3+2OH-
D.用NaOH溶液吸收氯气:Cl2+2OH—==2Cl—+H2O
 100分闯关期末冲刺系列答案
100分闯关期末冲刺系列答案 名校联盟快乐课堂系列答案
名校联盟快乐课堂系列答案科目:高中化学 来源: 题型:
向胶体中加入电解质能使胶体凝聚。使一定量的胶体在一定时间内开始凝聚所需电解质的浓度(a mol·L-1)称作“聚沉值 ”,电解质的“聚沉值”越小,则表示其凝聚力越大。实验证明,凝聚力主要取决于和胶体粒子带相反电荷的离子所带的电荷数,电荷数越大,凝聚力越大,则向Fe(OH)3胶体中加入下列电解质时,其“聚沉值”最小的是
”,电解质的“聚沉值”越小,则表示其凝聚力越大。实验证明,凝聚力主要取决于和胶体粒子带相反电荷的离子所带的电荷数,电荷数越大,凝聚力越大,则向Fe(OH)3胶体中加入下列电解质时,其“聚沉值”最小的是
A.NaCl B.FeCl3
C.K2SO4 D.Na3PO4
查看答案和解析>>
科目:高中化学 来源: 题型:
用惰性电极电解某溶液时,发现两极只有H2和O2生成,若电解前后温度变化忽略不计,则电解一段时间后,下列有关溶液叙述正确的有
①该溶液的pH可能增大②该溶液的pH可能减小③该溶液的pH可能不变④该溶液的浓度可能增大⑤该溶液的浓度可能减小⑥该溶液的浓度可能不变
A.①②③④⑤⑥ B.①②③④⑤
C.①②③④⑥ D.①②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关元素及其化合物性质的比较正确的是
A.原子半径:F<O<Al B.稳定性:H2O<PH3<NH3
C.酸性:H2CO3<H2SO4<H3PO4 D.碱性:LiOH<NaOH<Al(OH)3
查看答案和解析>>
科目:高中化学 来源: 题型:
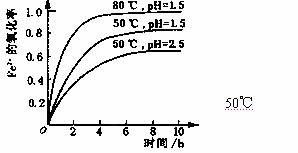
酸性溶液中,Fe2+会被空气缓慢氧化为Fe3+。不同条件下,一定浓度的Fe2+的氧化率随时间变化关系如右图所示。下列有关说法正确的是
A.该氧化过程的离子方程式为:
Fe2++O2+4H+===Fe3++2H2O
B.pH=1.5时Fe2+的氧化率一定比pH=2.5的大
C.Fe2+的氧化率仅与溶液的pH和温度有关
D.其他条件相同时,80℃时Fe2+的氧化率比50℃的大
查看答案和解析>>
科目:高中化学 来源: 题型:
氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产.生活中有着重要作用。请回答下列问题:
(1)用CH4 催化还原NOx 可以消除氮氧化物的污染。例如:
CH4(g) + 4NO2(g) = 4NO(g)+CO2(g) + 2H2O(g) ΔH1=-574 kJ·mol-1
CH4(g) + 4NO(g) = 2 N2(g)+CO2(g) + 2H2O(g) ΔH2、
若1 mol CH4 还原NO2 至N2,整个过程中放出的热量为867 kJ,则ΔH2= ;
(2)工业合成氨气需要的反应条件非常高且产量低,而一些科学家采用高质子导电性的SCY陶瓷(能传递H+ )实现氨的电化学合成,从而大大提高了氮气和氢气的转化率。电化学合成氨过程的总反应式为:N2+3H2 2NH3 ,则在电化学合成氨的过程中,正极反应式为 ;
2NH3 ,则在电化学合成氨的过程中,正极反应式为 ;
(3)在一定条件下,将l mol N2 与3 mol H2 混合于一个10 L密闭容器中,反应达到平衡时,A点混合气体中氨占25%,试回答:
①A点时N2的浓度为 mol/L;
 ②右图中在状态A时,平衡常数 KA =
②右图中在状态A时,平衡常数 KA =
(填写代入数值的表达式,不要求化简);当温度由T1变化到T2时,KA KB(填“>”、“ <”或“=”)。
③在容积固定的密闭容器中发生上述反应,各物质的浓度如下表:
| 时间/min 浓度/mol•L—1 | c (N2) | c (H2) | c (NH3) |
| 0 | 0.6 | 1.8 | 0 |
| 3 | 0.52 | x | 0.16 |
| 6 | 0.36 | 1.08 | 0.48 |
| 9 | 0.36 | 1.08 | 0.48 |
反应在3 min时,条件发生了改变,改变的条件可能是 (填序号)。
a.使用催化剂
b.降低温度
c.增加H2的浓度
d.充入Ne增大压强
查看答案和解析>>
科目:高中化学 来源: 题型:
2mol氢气和1 mol氧气化合生成2 mol液态水,放出571.6kJ热量。能正确表示这一反应的热化学方程式是
A.2H2 + O2 → 2H2O + 571.6kJ
B.2H2(g) + O2(g)→ 2H2O(g)+ 571.6Kj
C.2H2(g) + O2(g) → 2H2O(l) + 571.6kJ
D.2H2(g) + O2(g) → 2H2O(l) - 571.6kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
某晶体水溶液中加入Fe2+的溶液,再加稀硝酸溶液立即变红,另取 该晶体,加入NaOH溶液共热产生一种能使湿润红色石蕊试纸变蓝的气体,则这种晶体是
该晶体,加入NaOH溶液共热产生一种能使湿润红色石蕊试纸变蓝的气体,则这种晶体是
A.KSCN B.NH4SCN
C.NH4Cl D.FeCl3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com