
【题目】某届奥运会上,有个别运动员因服用兴奋剂被取消参赛的资格。下图是检测出兴奋剂的某种同系物X的结构,关于X的说法正确的是( )
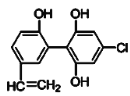
A. X分子中不可能所有原子都在同一平面上
B. X 遇到FeCl3溶液时显紫色,而且能使溴的四氯化碳溶液褪色
C. 1 mol X 与足量的浓溴水反应,最多消耗4 mol Br2
D. 1 mol X在一定条件下与足量的氢气反应,最多消耗1 mol H2
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】下表中对离子方程式的评价合理的是
选项 | 化学反应及其离子方程式 | 评价 |
A | H2SO4溶液与Ba(OH)2溶液反应: H++ SO42-+Ba2++OH | 正确 |
B | 向碳酸镁浊液中加入足量稀盐酸: CO32-+2H+ | 错误,碳酸镁不应写成离子形式 |
C | 向沸水中滴加饱和的氯化铁溶液至液体变为红褐色:Fe3++3H2O | 正确 |
D | 向NaOH溶液中通入少量CO2反应:OH+CO2 | 正确 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图,是实验室制备乙酸乙酯的装置。a试管中加入3mL95%的乙醇、2mL浓硫酸、2mL冰醋酸;b试管中是饱和碳酸钠溶液。连接好装置,用酒精灯对试管a加热,当观察到试管b中有明显现象时停止实验。
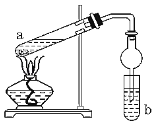
(1)在a试管中除了加入乙醇、浓硫酸和乙酸外,还应放入__,目的是__。
(2)试管b中观察到的主要现象是__。
(3)实验中球形干燥管除起冷凝作用外,另一个重要作用是__。
(4)饱和Na2CO3溶液的作用是__。
(5)反应结束后,将试管中收集到的产品倒入分液漏斗中,__、__,然后分液,得到乙酸乙酯。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一定量纯净的氨基甲酸铵(NH2COONH4)置于特制的密闭真空容器中(假设容器体积不变,固体试样体积忽略不计),在恒定温度下使其达到分解平衡:NH2COONH4(s)![]() 2NH3(g)+CO2(g)。
2NH3(g)+CO2(g)。
(1)下列不能判断该分解反应已经达到化学平衡状态的是___(填选项);
A.2v生(NH3)=v耗(CO2)
B.密闭容器中氨气的物质的量不变
C.容器中CO2与NH3的物质的量之比保持不变
D.密闭容器中总压强保持不变
E.形成6个N-H键的同时有2个C=O键断裂
(2)能使该反应的反应速率增大的是___(填选项);
A.及时分离出CO2气体
B.适当升高温度
C.加入少量NH2COONH4(s)
D.选择高效催化剂
(3)如图所示,上述反应中断开反应物中化学键吸收的能量___形成生成物中化学键放出的能量(填写“大于”“等于”“小于”)。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A是气态烃,完全燃烧时产生的CO2和H2O的物质的量之比为1∶1,A的相对分子量小于30,在下图变化中,中间产物C跟葡萄糖一样也能跟新制的Cu(OH)2发生反应产生砖红色沉淀,E有香味,(反应条件未写出)。
![]()
(1)写出下列各步变化的化学方程式(注明反应条件)
反应① _________________________________;
反应②__________________________________;
反应④__________________________________;
反应⑤__________________________________。
(2)写出下列反应类型:
反应① _____________________,反应② _____________________,
反应④ _____________________,反应⑤ _____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钯(Pd)、锌及其化合物在合成酮类物质中有极其重要的作用,如图为合成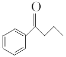 的反应过程:
的反应过程:
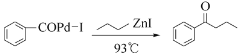
回答下列问题:
(1)I原子价电子排布式为___________,其能量最高的能层是___________(填能层符号)。
(2)H、C、O三种元素的电负性由大到小的顺序为___________。
(3) 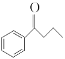 中碳原子的杂化方式为___________。
中碳原子的杂化方式为___________。
(4)ZnCl2溶液中加入足量氨水,发生的反应为ZnCl2+4NH3·H2O=[Zn(NH3)4]Cl2+4H2O。
①上述反应涉及的物质中,固态时属于分子晶体的是___________。
②NH3的空间构型为___________。
③1 mol [Zn(NH3)4]Cl2中含有___________mol σ键。
(5)Zn和Cu可形成金属互化物(ZnCu),该金属互化物中所有金属原子均按面心立方最密堆积,若所有Cu均位于晶胞的面心,则Zn位于晶胞的___________。
(6)金属钯的堆积方式如图所示:
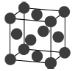
①该晶胞中原子的空间利用率为___________(用含π的式子表示)。
②若该晶胞参数a=658 pm,则该晶胞密度为___________(列出计算表达式)g·cm-3。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列几组物质:
①16O2和18O3②35Cl和37Cl-③金刚石和石墨④12C和16C⑤1H2O和D2O⑥CH4与C7H16⑦C2H4和C3H6⑧淀粉和纤维素⑨CH3CH2CH2CH3和![]() ⑩CH3CH(CH3)CH2CH2CH3和CH3CH2CH2(CH3)CHCH3
⑩CH3CH(CH3)CH2CH2CH3和CH3CH2CH2(CH3)CHCH3 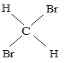 和
和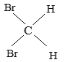
![]() 和
和![]()
(1)互为同位素___;
(2)互为同素异形体___;
(3)互为同系物___;
(4)互为同分异构体___;
(5)为同一物质___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为锌铜原电池示意图,下列说法错误的是( )
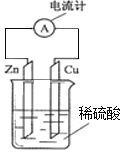
A.锌片为负极,且锌片逐渐溶解
B.电子由锌片通过导线流向铜片
C.铜为正极,铜不易失电子而受到保护
D.溶液中阳离子向![]() 极移动,且
极移动,且![]() 极上发生的是氧化反应
极上发生的是氧化反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚氯酸钠(NaClO2)在溶液中会生成ClO2、HClO2、ClO2-、Cl-等,其中HClO2和ClO2都是具有漂白作用。已知pOH=-lgc(OH-),经测定25℃时各组分含量随pOH变化情况如图所示(Cl-没有画出),此温度下,下列分析正确的是

A. HClO2的电离平衡常数的数值Ka=10-8
B. pOH=11时,ClO2-部分转化成ClO2和Cl-离子的方程式为:5ClO2-+2H2O=4ClO2+ Cl-+4OH-
C. pH=7时,溶液中含氯微粒的浓度大小为:c(HClO2)>c(ClO2-)>c(ClO2)>c(Cl-)
D. 同浓度的HClO2溶液和NaClO2溶液等体积混合,则混合溶液中有:c(Na+)+c(OH-)=c(H+)+ c(HClO2)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com