
以铬酸钾为原料,电化学法制备重铬酸钾的实验装置示意图如下:
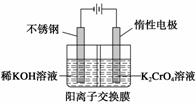
下列说法不正确的是( )
A.在阴极室,发生的电极反应为2H2O+2e-===2OH-+H2↑
B.在阳极室,通电后溶液逐渐由黄色变为橙色,是因为阳极区H+浓度增大,使平衡2CrO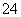 +2H+Cr2O
+2H+Cr2O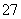 +H2O向右移动
+H2O向右移动
C.该制备过程中总反应的化学方程式为4K2CrO4+4H2O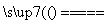 2K2Cr2O7+4KOH+2H2↑+O2↑
2K2Cr2O7+4KOH+2H2↑+O2↑
D.测定阳极液中K和Cr的含量,若K与Cr的物质的量之比(nK/nCr)为d,则此时铬酸钾的转化率为1-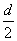
答案 D
解析 本题应结合电解的原理来具体分析、解决问题。
根据阴、阳离子的放电顺序可知,该电解池中的反应如下:
阴极:4H2O+4e-===2H2↑+4OH-、阳极:2H2O-4e-===O2↑+4H+,阳极区K2CrO4溶液中存在平衡:2CrO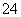 +2H+Cr2O
+2H+Cr2O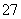 +H2O,H+浓度增大,使该平衡右移生成Cr2O
+H2O,H+浓度增大,使该平衡右移生成Cr2O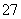 。故电解池中的总反应式可写成4K2CrO4+4H2O
。故电解池中的总反应式可写成4K2CrO4+4H2O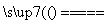 2K2Cr2O7+4KOH+2H2↑+O2↑。故A、B、C项均正确。
2K2Cr2O7+4KOH+2H2↑+O2↑。故A、B、C项均正确。
D项,设K2CrO4转化为K2Cr2O7的转化率为α,则:
2K2CrO4~K2Cr2O7
初始量 2 0
转化量 2α α
最终量 2-2α α
则有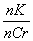 =
=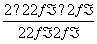 =d
=d
解得α=2-d,D项错误。


 阳光课堂同步练习系列答案
阳光课堂同步练习系列答案科目:高中化学 来源: 题型:
下列各图为元素周期表的一部分(表中数字为原子序数),其中正确的是( )
A
| 2 | 3 | 4 |
| 11 | ||
| 19 |
B
| 2 | ||
| 10 | 11 | |
| 18 | 19 |
C
| 6 | ||
| 1 | 12 | 13 |
| 24 |
D
| 6 | 7 | |
| 14 | ||
| 31 | 32 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于蛋白质的叙述正确的是( )
A.蛋白质均为天然高分子化合物
B.蛋白质均溶于水,加热能使其变性
C.蛋白质水解的最终产物是氨基酸
D.在蛋白质溶液中加入饱和硫酸铵溶液,析出的蛋白质的生理功能发生了改变
查看答案和解析>>
科目:高中化学 来源: 题型:
大豆含有大量的蛋白质和脂肪,由大豆配制出来的菜肴很多,它是人体营养中最重要的补品之一,我们几乎每天都要饮食豆制品。请回答下列问题:
(1)我们所吃的豆腐是一种________。
A.蛋白质凝胶 B.纯蛋白质
C.脂肪 D.淀粉
(2)我们食用的大豆,最终补充给人体的主要成分是________。
A.氨基酸 B.蛋白质
C.油脂 D.糖类
(3)天然蛋白质水解的最终产物是________,请以甘氨酸( )为例,写出其与NaOH反应的化学方程式:____________________________。
)为例,写出其与NaOH反应的化学方程式:____________________________。
(4)豆油不能保存较长时间的原因主要是________________________________,所以必须进行硬化,油脂的硬化是指________________________________________,人造脂肪指的是______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
根据以下三个热化学方程式:
2H2S(g)+3O2(g)===2SO2(g)+2H2O(l)
ΔH=-Q1 kJ·mol-1
2H2S(g)+O2(g)===2S(s)+2H2O(l)
ΔH=-Q2 kJ·mol-1
2H2S(g)+O2(g)===2S(s)+2H2O(g)
ΔH=-Q3 kJ·mol-1
判断Q1、Q2、Q3三者关系正确的是( )
A.Q1>Q2>Q3 B.Q1>Q3>Q2
C.Q3>Q2>Q1 D.Q2>Q1>Q3
查看答案和解析>>
科目:高中化学 来源: 题型:
化学反应中的能量变化,是由化学反应中旧化学键断裂时吸收的能量与新化学键形成时放出的能量不同所致。下图为N2(g)和O2(g)生成NO(g)过程中的能量变化:

(1)人们通常把拆开1 mol某化学键所吸收的能量看成该化学键的键能。键能的大小可以衡量化学键的强弱,则N≡N键的键能为____________kJ·mol-1。根据上图写出N2(g)和O2(g)生成NO(g)的热化学方程式:
________________________________________________________________________。
(2)NO(g)分解生成N2(g)和O2(g)的热化学方程式为________________;当有16 g O2(g)生成时,该反应中放出的热量为________kJ。
查看答案和解析>>
科目:高中化学 来源: 题型:
在恒温、体积为2 L的密闭容器中进行反应:2A(g)3B(g)+C(g),若反应物在前20 s由3 mol降为1.8 mol,则前20 s的平均反应速率为( )
A.v(B)=0.03 mol·L-1·s-1
B.v(B)=0.045 mol·L-1·s-1
C.v(C)=0.03 mol·L-1·s-1
D.v(C)=0.06 mol·L-1·s-1
查看答案和解析>>
科目:高中化学 来源: 题型:
某化学实验小组的同学为探究和比较SO2和氯水的漂白性,设计了如下的实验装置。
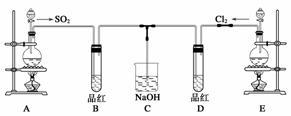
(1)实验室用装置A制备SO2。某同学在实验时发现打开A的分液漏斗活塞后,漏斗中液体未流下,你认为原因可能是________________________________________________
(2)实验室用装置E制备Cl2,其反应的化学方程式为:MnO2+4HCl(浓)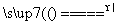 MnCl2+Cl2+2H2O。若有6 mol 的HCl参加反应,则转移的电子总数为_______________________;
MnCl2+Cl2+2H2O。若有6 mol 的HCl参加反应,则转移的电子总数为_______________________;
(3)①反应开始一段时间后,观察到B、D两个试管中的品红溶液出现的现象是:
B:____________________________________,D:______________________________。
②停止通气后,再给B、D两个试管分别加热;两个试管中的现象分别为:
B:____________________________________,D:________________________________。
(4)另一个实验小组的同学认为SO2和氯水都有漂白性,二者混合后的漂白性肯定会更强。他们将制得的SO2和Cl2按1∶1同时通入到品红溶液中,结果发现褪色效果并不像想象的那样。请你分析该现象的原因(用化学方程式表示)_______________________________
________________________________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com