
| A、Cl2 |
| B、CO2 |
| C、SO2 |
| D、CO |


科目:高中化学 来源: 题型:
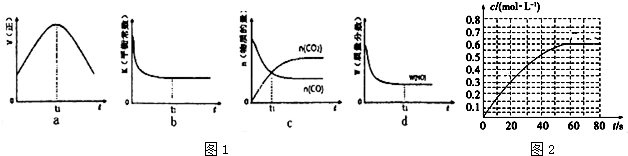
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
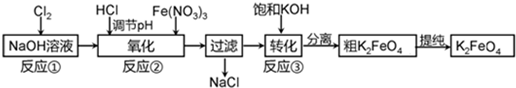
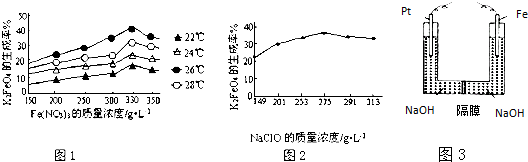
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、N、O、S、Si的原子半径逐渐增大,非金属性逐渐减弱 |
| B、SO2和SiO2既能与NaOH溶液反应,又能与某些酸反应 |
| C、N、S的氧化物既是形成光化学烟雾,又是形成酸雨的主要物质 |
| D、N、Si、S的单质均能和氧气反应,且产物分别是NO2、SiO2和SO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、分别加入BaCl2溶液 |
| B、向两种溶液中分别逐滴加入盐酸 |
| C、分别加入Ca(OH)2溶液 |
| D、分别取两种溶液,进行焰色反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、每生成1mol Fe3O4,反应转移的电子总数为2 mol | ||
| B、也可在酸性条件下用该方法制备Fe3O4纳米颗粒 | ||
C、反应每消耗1mol Fe2+,被Fe2+还原的O2的物质的量为
| ||
| D、x=2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
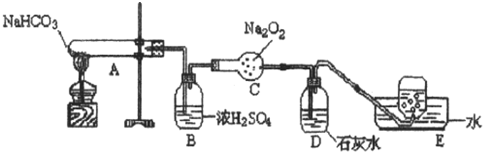
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、使用催化剂可以改变化学反应的活化能,但不改变反应的晗变 |
| B、Na2CO3溶液加水稀释后,恢复至原温度,pH和Kw均减小 |
| C、50℃时,pH=11的纯碱溶液中c(OH-)=1.0×10-3mol?L-1 |
| D、反应NH3(g)+HCl(g)=NH4Cl(s)在常温时向右进行,加热时向左进行,是因为该正向△H>0,△S<0 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com